概述
原人参二醇是一种白色结晶粉末,可溶于甲醇、乙醇、DMSO等有机溶剂,来源于人参。原人参二醇是二醇组皂苷的代谢苷元,可用作细胞凋亡诱导剂。
制备【1】【2】
1. 酸降解法
1966 年, Shibata 等发现盐酸能使人参皂苷Rc、Rb1和Rb2的混合物水解成原人参二醇。2003 年,陈业高等用浓盐酸在常温下对三七叶总皂苷进行水解,得到了20( R) -原人参二醇,产率为0.9%。研究表明,酸能使C-20羟基和侧链的双键脱水环合,形成C-20 手性不同的一对异构体20( S) -人参二醇和20( R) -人参二醇。且C-20 位的构型极易受酸的影响,发生互变异构现象,使得原人参二醇的产率降低。
2. 碱降解法
韩国学者通过直接碱降解人参叶皂苷得到了原人参二醇。Im 等在无水吡啶中用甲醇钠对韩国产人参中总皂苷进行碱降解,制得了原人参二醇,试验表明,反应具有专一性。Cui 等用正丁醇和甲醇钠对绞股蓝皂苷进行碱性裂解,通过气相色谱-质谱联用技术鉴定,得到了20( S) -原人参二醇。此外,王鹏豪等还将三七叶总皂苷溶于正丁醇钠- 正丁醇溶液中进行碱性氧化水解, 90 ℃通氧回流24 h,分离得到了原人参二醇,产率为0.2%。陈业高等采用2 mol /L 的NaOH 溶液在沸水浴环境中对三七叶总皂苷进行水解,得到了原人参二醇,产率为1%,该法比酸水解法反应温和,克服了酸降解法中产物易转变的缺点,且操作简单。李绪文等将西洋参茎叶总皂苷和NaOH 一同溶于甘油中,在常压和高温条件下进行降解,并通过正交试验确定了制备20( S) -原人参二醇的降解条件,最终20( S) -原人参二醇产率为5. 01%,纯度为98. 56%。该法具有产率和纯度高及成本低等特点。
3. Smith 降解法
3.1 降解过程
根据文献方法对三七总皂苷进行Smith降解。称取三七总皂苷1009,溶于水,加入433.5g过碘酸钠,室温搅拌12h,过滤。滤渣用适量甲醇溶解,加入35g四氢硼钠.静置过夜,加入1500ml。水稀释,用lmol/L硫酸调节溶液pH至2.0,使之水解,过夜。待水解完全后,用等体积氯仿萃取3次,合并氯仿层,回收氯仿,得到水解产物。
3.2 分离纯化
所得水解产物进行柱层析分离。用正相柱层析硅胶干法装柱,取水解产物,以适量二氯甲烷溶解,然后加入适量柱层析硅胶搅匀,静置至溶剂挥干,研细。将样品装于柱顶,用二氯甲烷乙酸乙酯(10:1~1:1)进行梯度洗脱,所得流份经TLC检测,合并相同组分,最终得到5个流份AtE。各流份经反复硅胶柱层析、制备HPLC、重结晶等方法,得化合物I~Ⅸ。具体分离流程见下图。
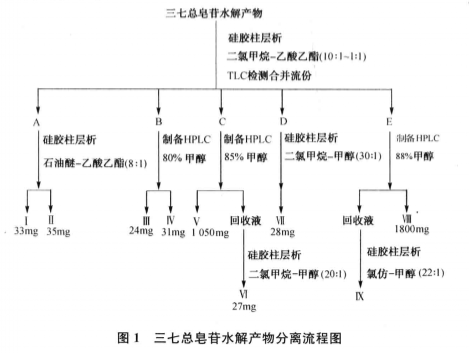
4. 微生物转化法
Akao 等研究表明,大鼠血浆中肠内菌代谢人参皂苷Rb1后可得到原人参二醇。陈昕等通过离体及整体试验观察了人和大鼠肠内菌对人参皂苷Rb1( GRb1) 的代谢,采用薄层色谱(TLC) 和电喷雾质谱( ESI-MS) 检测G-Rb1及其代谢产物。结果表明,G-Rb1可被人和大鼠肠内菌代谢,其代谢模式为G-Rb1→Rd→F2→compound K( CK,20S-protopanaxadiol 20-O-β-D-glucopyranoside) →20( S) -原人参二醇。
Qian 等对人参皂苷Rb1、Rg3和Rh2在小鼠胃肠道内的代谢研究表明,氧合和去糖基化是2 种主要的代谢途径,并且发现3 种皂苷的代谢产物中均有原人参二醇,进一步说明肠道内的细菌能将人参皂苷代谢为其对应的苷元。马吉胜等在恒温振荡条件下,选取10 种有潜在β-葡糖苷酶分泌能力的真菌对人参皂苷Rb1及人参二醇系皂苷( PDS) 进行代谢试验,结果表明,6种真菌的代谢产物中均存在原人参二醇,其代谢模式为G-Rb1( 或PDS) →G-Rd→G-F2→CK→原人参二醇。研究者将从土壤中提取的天然曲霉菌( Aspergillus niger) 与含Rg3的黑人参提取物在50 ℃的温度下混合、反应,最终得到了20( R) -原人参二醇和20( S) -原人参二醇。并通过HPLC 检测,确定了反应过程为: Rg3( S)→Rh2( S) →PPD( S) 和Rg3( R) →Rh2( R) →PPD( R)。从激烈热球菌中得到的对热稳定的β-糖苷酶能将人参皂苷Rd 和人参根部提取物( Rb1、Rb2、Rc) 经compound K 降解为原人参二醇,并确定了反应条件。该法的原人参二醇产率在目前的研究中是最高的。综上可知,微生物降解反应具有高度的立体选择性、反应条件温和、设备简单、公害少、反应速率快等特点。但其转化条件进行优化和菌种的选择需要进一步筛选研究,以寻找微生物及其反应条件,以达经济效益。
原人参二醇的结构改造【3】【4】
1. 化学法
1.1 氧化和还原反应
Shibata 等对原人参二醇和异原人参二醇的混合物进行了酯化、催化氢化等操作,得到了含有酯基的原人参二醇和二氢原人参二醇,还由原人参二醇和异原人参二醇制得了人参二醇。Wang 等先用还原剂将( H2,Pt-C) 原人参二醇还原为20R-二氢原人参二醇,再用PCC 将二氢原人参二醇3、12 位的羟基氧化成酮。吴久伟等根据原人参二醇在氯仿与水中的溶解度差异,用酸性重铬酸钾溶液与其氯仿溶液进行反应,制得原人参二醇氧化物,然后用新制的硼氚化钠氚化还原合成原人参二醇。所得产物经高效液相色谱纯化后,放射化学纯度大于98%,放射性比活度达738 GBq /mmol,各项指标能满足医药学相关研究的要求。Meng 等改变还原条件,采用硼氚化钠在N,N-二甲基乙酰胺中,选择性地使原人参二醇反应生成[3-3H]原人参二醇,产率达22%,放射性成分提纯可达99%,C-3 /C-12 上放射性标记比率为97∶3。
2. 成苷反应
Atopkina等以原人参二醇为起始物,通过氧化、糖基化、催化加氢、酰化等一系列反应,得到了多种苷类物质。
3. 酶、微生物转化法
Wang 等发现分歧杆菌( Mycobacterium.sp. ) 能将原人参二醇转化为12,20R-dihydroxydammaran-3-one 和12β, 20R, 25-trihydroxydammaran-3-one,产率分别为24. 7% 和1. 4%。在研究人参皂苷Rb1、Rg3和Rh2在小鼠胃肠道内的微生物转化时发现,3种皂苷均能被代谢成原人参二醇,原人参二醇能继续被氧化成单氧原人参二醇( MW 为476) 或二氧原人参二醇( MW 为492)。研究还发现,原人参二醇在原人参二醇6 位羟化酶和还原型辅酶Ⅱ作用下能转化成原人参三醇。北京大学药学院Li 等用刺状毛霉菌AS 3. 3450 对20( S) -原人参二醇进行生物转化,得到了8 个原人参二醇的衍生物,其中6 个为新化合物,该生物合成反应克服了化学合成中的诸多难题。
参考文献
[1] 陈业高,吕瑜平,桂世鸿,等. 三七叶甙制备原人参二醇及其差向异构体[J]. 精细化工,2003.07,第425页
[2] 南通大学教务处主编,学海图南 南通大学优秀毕业设计(论文)集 2010届,苏州大学出版社,2013.08,第444页
[3] 李宁,高露莎,黄媛,等. 两个新的20(S)-原人参二醇油酸酯衍生物[J]. 中国药物化学杂志,2008.01,第60页
[4] 胡晓琴,蒋金和,马永杰,陈业高,原人参二醇的制备与结构改造研究进展,安徽农业科学,Journal of Anhui Agri. Sci. 2012.10, 第5880页
