背景及概述[1][2]
1-环丙基-6-氟-1,4-二氢-4-氧代-7-( 1-哌嗪基) -3-喹啉羧酸盐酸盐一水合物(盐酸环丙沙星) 是喹诺酮类抗菌药物中抗菌活性最强的一个化合物。盐酸环丙沙星是德国 bayer 公司于 1983 年研制的氟喹诺酮类抗菌优秀药物,具有广谱抗菌作用,用于泌尿生殖系统感染、呼吸道感染、胃肠感染、禽霍乱、禽伤寒、骨和关节感染、皮肤软组织感染、败血症等。通过抑制细菌 DNA 旋转酶,使 DNA 复制、合成、转录、修复受理而起到抑菌作用。因其广谱,副作用小,高效且价廉,已在多国上市,成为世界畅销药。
现在较为普通的工业化方法是以环丙羧酸为原料,合成方法有直接取代法、先取代再水解法、先取代再脱水及先制中间体,再经取代、水解 制得。以环丙羧酸与 N-乙氧羧苯哌嗪在DMSO 溶剂中反应,然后水解,再成盐制得,总效率97%,步骤多,成本高,不适于工业生产。以环丙羧酸与哌嗪直接反应,然后成盐,步骤简单,但总效率只有 81.6% 。以环丙羧酸与哌嗪在乙二醇单甲醚中反应,然后成盐,步骤简单,总收率有 101.3%,但哌嗪用量太大。
以环丙羧酸与哌嗪在 DMF 溶剂中反应,成盐,所用溶剂较多,步骤繁烦,收率有 109.4%,但哌嗪用量太多。以二水哌嗪在水相中合成环丙沙星,工艺繁烦,工业化不适用,但提供了新思路。以环丙羧酸与无水哌嗪反应,采用了多种溶剂,环丙沙星不经精制,直接成盐,结晶,所含杂质成分较多,收率 100%左右,有一定价值。
作用和用途[3]
盐酸环丙沙星为第三代喹诺酮类抗菌药。其主要作用机制是抑制参与核酸合成的DNA回旋酶,通过破坏细菌DNA结构而阻止细胞分裂而杀菌。口服生物利用度约为52%(因有首过效应),服药后85分钟血药浓度可达峰值。静注本品,半衰期为2.8~4.2小时。本品易渗入许多组织,其组织浓度高于血清浓度,并且广泛分布于各种体液和脏器,静注后在骨皮质及网状骨质中的浓度较高。
口服和静注后部分由肝脏代谢,主要以原形自尿和粪便中排泄。本品是氟喹诺酮类药物中抗菌力最强的药物。抗菌谱广、抗菌活性强,对革兰阳性菌和阴性菌均有抗菌作用。尤其对肠杆菌如大 肠埃希菌、肺炎克雷伯杆菌等尤为突出,对铜绿假单胞菌、金黄色葡萄球菌等也有良好的抗菌作用,但肺炎链球菌及A组链球菌则对之不甚敏感,对厌氧菌的活性也较低。
盐酸环丙沙星适用于敏感菌引起的尿路感染、中度及重度呼吸道感染、肠道感染、皮肤软组织感染、败血症与腹腔内感染等。
药代动力学[4]
盐酸环丙沙星口服生物利用度为49%~ 70%,服药后1~ 2小时血药浓度可达高峰。其分布及组织穿透性良好,在胆汁、肾脏、胆囊和肝脏、肺部、女性生殖器官、前列腺组织液中浓度较高。绝大部分以原形经尿液排泄,其余药物经胆汁和粪便排出。
不良反应[5]
盐酸环丙沙星常见恶心、腹泻、呕吐、腹痛、腹胀、伪膜性肠炎、头晕、头痛、疲劳、激动、震颤。可有味觉受损、视觉紊乱、耳鸣、听觉暂时损伤、皮肤过敏反应、药物热、皮肤出血及血管炎,严重者可致间质性肾炎、肝炎、肝坏死、血管喉头水肿及过敏性休克;少见失眠、外周感觉异常、出汗、惊厥、颅内压升高、焦虑、精神错乱、抑郁。
个别出现精神反应如自残行为,其他有心动过速、潮红、偏头痛、晕厥、关节痛、无力、肌肉痛、腱鞘炎、光敏感及暂时肾功 能损害,偶见跟腱炎及跟腱断裂;血液有嗜酸粒细胞增多,白细胞减少,贫血,血小板减少及凝血机制异常,可引起转氨酶升高、胆汁淤积性黄疸及高血糖、结晶尿或血尿;注射局部可致静脉炎或血栓性静脉炎。
对本品或其他喹诺酮类过敏者禁用。儿童、青少年及妊娠、哺乳期妇女禁用。癫痫和患有中枢神经系统疾病者慎用;肝、肾功能不全者减少用量;可影响反 应能力,尤其在饮酒时更为显著;与茶碱类药物同用可致血茶碱浓度升高;与某些非甾体类抗炎药合用可引起惊厥,可增强华法林和优降糖的作用,丙磺舒可干扰本药肾代谢。
剂量和用法[3]
片剂:环丙沙星单水盐酸盐,每片含本品250mg、500mg。 口服每次250mg,每日2次,重症者可加倍量,但每日最高量不可超过 1500mg,肾功能不良(肌酐清除率低于30ml/min)应减少用量。注射剂:环丙沙星乳酸盐,100mg/50ml、200mg/100ml。先用等渗氯化钠或葡萄糖注射液稀释。静滴,每次200mg,每日2次,治疗尿路感染每次100mg,每12小时1次,静脉滴注,滴注时间不少于30分钟。
注意事项[6]
1. 对喹诺酮类药物过敏者禁用。
2. 孕妇、哺乳期妇女及16岁以下小儿禁用。
药物相互作用[5]
1. 严重抑制茶碱的正常代谢,联合应用可引起茶碱的严重不良反应。
2. 抗酸药可抑制本品的吸收,致使血尿中药物浓度降低,应避免同时使用。
制备 [2,4-5]
方法1:以氟氯苯乙酮( 2,4-二氯-5-氟苯乙酮) 为起始原料,与碳酸二乙酯缩合得 2,4-二氯-5-氟苯甲酰乙酸乙酯,再用原甲酸三乙酯烯化,环丙胺胺化得 2-( 2,4-二氯-5-氟苯甲酰) -3-环丙基胺基丙烯酸乙酯,最后经环合、引入哌嗪基、成盐而得到环丙沙星。反应路线如下:
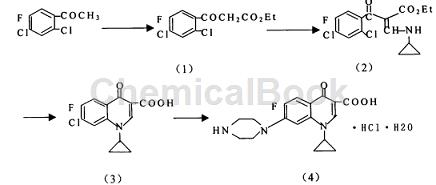
具体步骤如下:
步骤1:2,4 二氯-5-氟苯甲酰乙酸乙酯( 1) 的合成:于 250 mL 反应瓶中加入甲醇钠 21.6 g( 0.40 mol),蒸干呈白色粉状固体,加碳酸二乙酯 45 g,升温至回流,滴加 2,4-二氯-5-氟苯乙酮 10.3 g( 0.05 mol) 与 30 mL 碳酸二乙酯组成的混合物,回流反应 3 h,并不断蒸出生成的乙醇。反应毕,减压除去碳酸二乙酯,残余物加水 40 m L,环己烷 35 m L,冷至 15 ℃以下,滴加浓盐酸 25 m L,升温回流 20 min,冷却分层,环己烷层用水洗涤,水层用环己烷10 m L 、5 m L 提取 2 次,合并环己烷层,干燥,过滤,室温干燥得产品 12.8 g,收率 92.22 %.
步骤2:2-( 2,4-二氯-5-氟苯甲酰) -3 环丙基胺基丙烯酸乙酯( 2) 的合成:
于 250 mL 反应瓶中加入( 1) 28.0 g( 0.10 mol),原甲酸三乙酯 22.2 g( 0.15 mol) 及乙酐 30.6 g( 0.30mol),搅拌下缓缓升温至 140 ℃反应 3 h,减压除去生成的乙醇,向残余物中加入无水乙醇 120 mL,在 0 ℃左右滴加环丙胺 8.6 g( 0.15 mol),加毕室温反应 1.5 h,抽滤,重结晶,得 27.8 g,收率 80.07 %,m p89 ℃~90 ℃。
步骤3:1-环丙基-7-氯-6-氟-1,4-二氢-4-氧代喹啉-3-羧酸( 3) 的合成:于 250 mL 反应瓶中依次加入( 2) 17.3 g( 0.05 mol),碳酸钠 8.5 g( 0.08 mol),DMF100 mL,加毕,回流反应 1.5 h,蒸出 DMF,残余物加氢氧化钠 6 g( 0.15 mol),纯化水 80 mL,回流反应 2 h,热过滤,滤液用盐酸酸化至 pH1 ~ 2,抽滤,用正丁醇与水的混合物洗涤,干燥得 13.1 g,收率93.03 %,熔点 234 ℃~ 237 ℃。
步骤4:1-环丙基-6-氟-1,4-二氢-4-氧代-7-( 1-哌嗪基) -3-喹啉羧酸盐酸盐一水合物( 4) 的合成::于 500 mL 反应瓶中加入( 3) 18.0 g( 0.06394 mol),无水哌嗪 27.5 g( 0.3198 mol),DM F80 mL,搅拌下缓缓升温回流,反应 5 h 后,减压蒸除 DM F.残余物加 10 %氢氧化钠溶液 70 mL,升温至 80 ℃加活性炭脱色,过滤,滤液加异戊醇 200 m L,用酸中和,冷却至 15 ℃过滤。
滤液冷却至 10 ℃以下回收哌嗪,回收所得六水哌嗪,加异戊醇蒸馏除水得无水哌嗪,可用于下批反应; 滤饼用水洗净,抽干,加酸溶解,用氢氧化钠溶液中和,冷却,过滤,洗涤,滤饼加 95 %乙醇 200 m L,升温回流,滴加盐酸至 pH1~ 2,经过滤 、洗涤、干燥,得白色结晶 19.7 g,收率 76%。
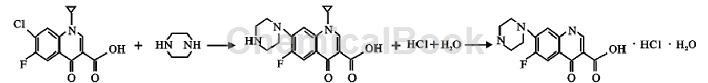
方法2:环丙羧酸( 1-环丙基- 7-氯- 6-氟- 1,4-二氢- 4-氧化喹啉- 3-羧酸) 和哌嗪发生亲核取代反应生成环丙沙星,再与盐酸成盐生成盐酸环丙沙星。考察了溶剂类型、反应时间、温度、溶液碱度、纯化方式等因素对产品收率和含量的影响。结果表明,工艺条件为: 环丙羧酸与无水哌嗪的质量比为 1 ∶ 0.9,在 130 ℃ 反应 7 h,收率可达 98.9%,含量 99.6%,该工艺成本低,收率高,含量高,具有工业化应用前景。
主要参考资料
[1] 李灵芝, 陈海宽, 刘巧云, & 李祖文. (2003). 盐酸环丙沙星的合成及工艺改进. 山西大学学报: 自然科学版, 26(3), 241-243.
[2] 盐酸环丙沙星合成工艺研究
[3] 临床常用药物
[4] 口腔临床药物手册
[5] 常用新药精汇手册
[6] 全科医生药物手册
