背景[1-3]
人卵巢腺癌细胞源自一名60岁白人女性卵巢肿瘤组织,由T.C.Hamiltonyu建系于1982年。该细胞带有雌、雄激素受体。对阿霉素,顺氯氨铂,(左旋)苯丙氨酸氮芥有一定抗药性,适用于卵巢癌的抗药性研究。OVCAR-3染色体数量在亚三倍体范围内。
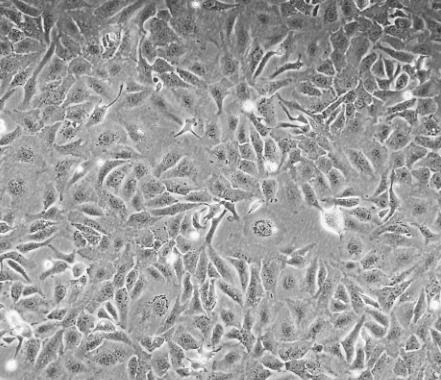
人卵巢腺癌细胞
人卵巢腺癌细胞培养方法:
1、人卵巢腺癌细胞传代:细胞密度达到80-90%时即可传代
①弃去培养上清,用PBS或生理盐水清洗1-2次;
②加入2ml0.25%胰酶(T25瓶),使胰酶覆盖整个瓶或皿,盖好放入培养箱消化;
③1-2min后,显微镜下观察细胞,若大部分细胞回缩且有少量细胞脱落,轻轻吹打下确认消化情况后加入完全培养基终止消化;若细胞还是贴壁,放回培养箱继续消化至可以轻轻吹打下为止;
④将人卵巢腺癌细胞悬液1000RPM左右条件下离心4min,弃上清;
⑤用新鲜培养基重悬后加入培养瓶或皿中,T25培养瓶加6-8ml培养基;
⑥悬浮细胞直接离心收集,细胞沉淀重悬后分到新培养瓶中。
2、人卵巢腺癌细胞复苏:
①将冻存管在37℃温水中快速摇晃融化,时间1min左右,加入4-5ml培养基混匀。
②在1000RPM左右条件下离心4min,弃上清,加1-2ml培养基吹匀,将细胞悬液加入培养瓶中,补加适量培养基。
3、人卵巢腺癌细胞冻存:待细胞生长状态良好时进行细胞冻存保种
①弃去培养上清,用PBS或生理盐水清洗1-2次,加入1mL 0.25%胰蛋白酶(T25瓶)
②1-2min后,显微镜下观察细胞,大部分细胞回缩且有少量细胞脱落,轻轻吹打下确认消化情况后加入完全培养基终止消化;
③将人卵巢腺癌细胞悬液1000RPM左右条件下离心4min,弃上清,加1ml冻存液重悬细胞;
④将冻存管放入程序降温盒,放入-80℃冰箱,4小时后将冻存管转入液氮罐储存。
应用[4][5]
人卵巢腺癌细胞可以用于CircRNA-657编码新型多肽与GLI1互作促进卵巢癌细胞干性形成
研究拟发现对OCSCs干性维持具有重要作用的circ RNA,并深入探究其调控OCSCs干性的机制,旨在发现新的逆转卵巢癌恶性进展的靶点。
方法:1.OCSCs的诱导与鉴定:采用无血清非黏附悬浮培养OVCAR3和CAOV3卵巢癌细胞株,富集传代形成具有干性的球囊细胞OVCAR3 S和CAOV3 S,并通过q RT-PCR、流式细胞术、有限梯度稀释实验等验证其干细胞特性。
2. Circ657的表达与成环验证:对OVCAR3和OVCAR3 S细胞以及卵巢上皮细胞HOSEpic(HOSE)样本进行基因芯片微阵列的差异分析,筛选出OVCAR3 S细胞中高表达的circ RNA657(circ657)。并通过q RT-PCR、稳定性实验、酶切实验验证circ657在卵巢癌细胞系中的表达情况以及它的环状情况。
3. Circ657编码多肽能力评估:通过生物信息学软件预测circ657是否具备编码多肽的条件,并通过q RT-PCR和Western Blot对circ657翻译多肽的功能进行鉴定。
4. Circ657调控OCSCs干性考察:在OVCAR3和CAOV3卵巢癌细胞株构建circ657过表达载体,在OVCAR3 S卵巢癌球囊细胞构建circ657沉默载体;采用CCK8、平板克隆形成实验、transwell迁移实验检测circ657对卵巢癌细胞的增殖、克隆形成能力、迁移能力等干性特性的影响。
5. Circ657调控OCSCs干性机制探究:在OVCAR3和CAOV3卵巢癌细胞株构建circ657过表达载体,通过免疫荧光共定位实验检测circ657编码的多肽与GLI1的细胞定位情况,通过co-ip实验验证circ657编码的多肽与GLI1结合情况,进而探究circ657调控OCSCs干性的机制。
结果:1.OVCAR3 S和CAOV3 S细胞具有OCSCs干性特性:通过OVCAR3和CAOV3诱导富集形成的OVCAR3 S和CAOV3 S细胞干细胞表面标志物CD133表达升高,迁移能力和单克隆细胞球形成能力增强,具有干性特性。
2. Circ RNA-657在OCSCs中稳定存在并高表达:初步筛选出的circ657在OVCAR3 S和CAOV3 S细胞中显著高表达,且对Rnase R酶消化具有抵抗,环状结构稳定。
3. Circ657具有编码多肽的能力:circ657拥有开放阅读框以及IRES元件,能够翻译多肽且翻译的多肽序列由166个氨基酸组成。
4. Circ657通过编码多肽促进卵巢癌细胞增殖迁移等干性:过表达circ657的OVCAR3和CAOV3细胞中细胞增殖、迁移能力明显升高,而沉默circ657的OVCAR3 S细胞中细胞增殖、迁移能力明显降低;并且这种对细胞增殖迁移的干性特性的调控是通过其编码的多肽介导的。
5.Circ657编码的多肽可能通过与GLI1互作调控卵巢癌细胞干性:circ657编码的多肽能够与GLI1直接结合,可能通过GLI1促进卵巢癌的干性,介导卵巢癌的发生与发展。
参考文献
[1]Circular RNA circIPO11 drives self-renewal of liver cancer initiating cells via Hedgehog signaling[J].Gu Yang;Wang Yanying;He Luyun;Zhang Jiahang;Zhu Xiaoxiao;Liu Nian;Wang Jianyi;Lu Tiankun;He Lei;Tian Yong;Fan Zusen.Molecular Cancer,2021(1)
[2]Hedgehog/GLI Signaling Pathway:Transduction,Regulation,and Implications for Disease[J].Sigafoos Ashley N.;Paradise Brooke D.;FernandezZapico Martin E..Cancers,2021(14)
[3]HNRNPL Circularizes ARHGAP35 to Produce an Oncogenic Protein[J].Yan Li;Bing Chen;Jingjing Zhao;Qin Li;Siyuan Chen;Tianan Guo;Yuchen Li;Hongyan Lai;Zhiao Chen;Zhiqiang Meng;Weijie Guo;Xianghuo He;Shenglin Huang.Advanced Science,2021(13)
[4]Circular RNA-encoded oncogenic E-cadherin variant promotes glioblastoma tumorigenicity through activation of EGFR–STAT3 signalling[J].Gao Xinya;Xia Xin;Li Fanying;Zhang Maolei;Zhou Huangkai;Wu Xujia;Zhong Jian;Zhao Zheng;Zhao Kun;Liu Dawei;Xiao Feizhe;Xu Qiang;Jiang Tao;Li Bo;Cheng Shi Yuan;Zhang Nu.Nature Cell Biology,2021(3)
[5]孙晓雨.CircRNA-657编码新型多肽与GLI1互作促进卵巢癌细胞干性形成[D].中国医科大学,2022.
