概述[1]
hepes缓冲液的主要成分是羟乙基哌嗪乙硫磺酸(2-[4-(2-Hydroxyethyl)-1-piperazinyl]ethanesulfonic acid),HEPES是一种非离子两性缓冲液,其在pH 7.2 - 7.4 范围内具有较好的缓冲能力。其优点是在开放式培养或细胞观察时能维持较恒定的PH值.在这种培养条件下,细胞培养瓶的盖子应拧紧,以防止培养液中所需的少量碳酸盐散入空气中。
大多数培养液中含有酚红作为pH指示剂,酸性培养液呈橙黄色,碱性培养液呈深红色.HEPES有些昂贵,在高浓度时对一些细胞可能有毒. 原则上,hepes缓冲液可用来代替碳酸氢盐,以解除需要高浓度CO2培养环境的限制.实际操作中并非如此简单。溶解的CO2与碳酸氢盐对良好的细胞生长也是很重要的。
hepes缓冲液使用方法有两种:
(1)hepes缓冲液可按所需的浓度直接加入到配制的培养液中,再过滤除菌.每1000ml培养液中加入2.38克HEPES,待溶后用lN NaOH 调pH至7.2,滤过除菌后使用.此时HEPES的使用浓度为10 mmol/L.
(2)亦可配成 100 x 贮存液(l mol/L),使用前取 99ml培养液加入 lml贮存液,最终应用浓度仍为10mmol/L。l mol/L(100 x)hepes缓冲液配制方法:取23.8g HEPES溶于90ml双蒸水中,用lN NaOH调pH至7.5一8.0,然后用水定容至100ml,过滤除菌,分装小瓶(2ml/瓶),4℃或-20℃保存.
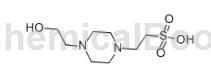
羟乙基哌嗪乙硫磺酸
应用[3]
1.促进脱矿牙本质再矿化的方法,包括以下步骤:
(1)将133mmol/L NaCl溶液加入到50 mmol/L乳酸溶液中,直至乳酸溶液的pH值为4,得 到配置好的乳酸溶液;将2mm×2mm×12mm大小的EBPM-NACP树脂条放置于50mL配置好的乳 酸溶液中,共放置42天;其中于第7、14、21、28、35、42天分别测量该乳酸溶液中的Ca、P离子 浓度,得到其初次释放曲线,即图1-2;随后,树脂条再置于100mL上述配制的乳酸溶液中30 天,使其树脂条中的Ca、P离子彻底释放;
(2)将步骤(1)中得到的树脂条浸泡于5mL CaCl2和HEPES缓冲液构成的pH值为7的溶液 中,其中CaCl2终浓度为100mmol/L,HEPES终浓度为50mmol/L,震荡1min,用去离子水冲洗树 脂条并于空气中干燥;对EBPM-NACP树脂条进行钙离子“充电”;
(3)将步骤(2)中得到的树脂条浸泡于5mL K2HPO4和hepes缓冲液构成的pH值为7的溶 液中,其中K2HPO4终浓度为60mmol/L,HEPES终浓度为50mmol/L,震荡1min,用去离子水冲洗 树脂条并于空气中干燥;对EBPM-NACP树脂条进行磷离子“充电”;
(4)重复步骤(2)和(3)三次,将树脂条冲洗1min并在空气中干燥;
(5)将步骤(4)处理得到的树脂条放置脱矿牙本质样本上,并置于模拟口腔环境中。
进一步的,步骤(5)处理之前还包括以下步骤:将脱矿牙本质样本用浓度为1mg/mL 的端基为氨基的聚酰胺-胺型树枝状聚合物溶液浸泡处理1h;端基为氨基的聚酰胺-胺型树 枝状聚合物采用第三代端基为氨基的聚酰胺-胺型树枝状聚合物,简称PAMAM;常温、常压下 将10mgPAMAM粉末溶于10ml去离子水中得到1mg/mL的PAMAM溶液;第三代端基为氨基的聚酰 胺-胺型树枝状聚合物是以乙二胺为起始核心,反复与丙烯酸甲酯通过Michael加成反应后 再与乙二胺通过酰胺化反应制备而成的。
2.制备纳米金颗粒
步骤S1:配制浓度为0.05-10mmol/L的氯金酸溶液;
步骤S2:配制浓度为5-50mmol/L的hepes缓冲液,并用氢氧化钠调节hepes缓冲液的PH值至7.0-8.0;
步骤S3:向步骤S2所配制的HEPES缓冲液中添加表面活性剂,配制浓度为1-2mmol/L的表面活性剂溶液;
步骤S4:将步骤S3所配制的表面活性剂溶液引入反应池,按氯金酸溶液和表面活性剂溶液的摩尔比为1:1-1:10向反应池中缓慢添加步骤S1所配制的氯金酸溶液,并以200-300r/min的速度匀速搅拌,反应5-30min,获得含有纳米金胶体的混合液;
步骤S5:将步骤S4所配制的混合液进行纳米金胶体的干燥提纯,获得纳米金颗粒。
以配制200L的浓度为50mmol/L的hepes缓冲液为例,其配置方法为:首先称取2.38kg的HEPES溶于180L的去离子水中,超声、振荡直至完全溶解;然后使用PH计测得此时溶液的PH值约为5.4,于是慢慢添加0.1mol/L的氢氧化钠溶液并不断搅拌直至PH调整至7.4;最后继续添加去离子至200L。
制备 [2]
方法1:
直接使用1,2-二氯乙烷作为溶剂,在装有机械搅拌、温度计的100mL的三口瓶中加入羟乙基哌嗪(5.00g,0.02mol),碳酸钾K2CO3(6.00g,0.04mol),50mL1,2-二氯乙烷,油浴加热90℃(1,2-二氯乙烷沸点85℃),搅拌反应20h。停反应,过滤,用200mL乙酸乙酯(EA)洗涤滤出的盐。滤液旋干,得2.6gHEPES固体。
方法二:
在装有磁力搅拌器、回流冷凝管的三口瓶中依次加入11.0g(84.5mmol)无水亚硫酸钠、27.0mL(343.6mmol)二氯乙烷、120mL水、110mL乙醇,50mg铜粉,搅拌,油浴加热升温到回流。回流22h后,将反应液减压蒸除水,至白色固体全部析出。此固体主要由产物、未反应的原料和生成的盐组成。将所得固体及500mL乙醇加入1L烧瓶中,加热回流40min。趁热抽滤,滤液冷却后,0℃放置过夜。抽滤,真空干燥,得片状结晶,产量11.40g,收率81.0%。
在装有磁力搅拌器、回流冷凝管、温度计的四口瓶中依次加入氯乙磺酸钠(15.10g,0.08mol),羟乙基哌嗪(9.88g,0.075mol),60mL水,油浴105℃搅拌反应,随着反应进行,反应液的pH会下降,滴加5mol/LNaOH水溶液,控制pH在9左右,共计加入15mL,再继续反应5h。
反应结束,将反应液加水稀释到500mL,上离子交换树脂柱(约500g)进行去盐纯化,反应液全部上柱之后,用蒸馏水冲至流出液pH为6,再用1mol/L氨水淋洗,收集TLC检测有产物点的流出液(pH约5~9)。旋蒸浓缩至150mL,加入活性炭脱色,油浴110℃,加热搅拌0.5h,过滤,旋干滤液,加入50mL乙醇,加热回流0.5h,热过滤,所得白色固体干燥后为8.63g。滤液滴加冰醋酸,调pH到5,0℃冷却过夜,过滤,所得固体干燥后为2.80g。与前述HEPES固体共计11.43g,收率64.5%。
10mmol/L hepes缓冲液配制方法如下:准确称取HEPES 2.383g,加入新鲜三蒸水定容至1L。过滤除菌,分装后4℃保存。如果用于加入细胞培养液中作缓冲剂,建议培养液避光保存。
主要参考资料
[1] 曾琦斐. (2010). 表面活性剂存在下hepes缓冲溶液中制备纳米金颗粒. 武汉工程大学学报, 32(7), 39-42.
[2] 缪骥, 马锋, 刘学民, 向俊西, 董鼎辉, & 吕毅. (2015). 低渗hepes缓冲溶液对腹腔内游离肝癌细胞杀伤作用的实验研究. 中国普外基础与临床杂志(1), 55-59.
[3] Morgia F, Torti M, Montigiani M, M. Sbracia, & 朱亮. (2006). 卵母细胞单精子显微注射过程中使用含有羟乙基哌嗪乙磺酸(hepes)的缓冲液对体外受精的结局有害. 世界核心医学期刊文摘:妇产科学分册(11), 31-32.
