【药品名称】
通用名称:安立生坦片
商品名称:凡瑞克 VOLIBRIS
英文名称:Ambrisentan tablets
汉语拼音:An Li Sheng Tan Pian
【成份】
化学名称:(+)-(2S)-2-[(4,6-二甲基嘧啶-2-基)氧基]-3-甲氧基-3,3-二苯基丙酸
化学结构式:
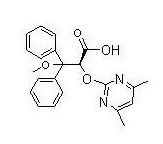
分子式:C22H22N2O4
分子量:378.42
【性状】
5mg片为粉红色双凸的方形薄膜衣片,一面刻有"GS",另一面刻有"K2C";
10mg片为深粉红色双凸的椭圆形薄膜衣片,一面刻有"GS",另一面刻有"KE3"
【用法用量】
本品应由有治疗肺动脉高压丰富经验的医生决定是否开始本药治疗,并对经验的医生决定是否开始本药治疗,并对疗过程进行严格监测。
1.成人剂量
起始剂量为空腹或进餐后口服5mg每日1次;如果耐受则可考虑调整为10mg每日1次。
药片可在空腹或进餐后服用。不能对药片进行掰半、压碎、或咀嚼。没有在肺动脉高压患者中进行过高于10mg每日1次剂量的研究。在开始使用本药治疗前和治疗的过程中要进行肝功能的监测(见【注意事项】部分)。
2.育龄期女性
女性只有在妊娠测试阴性、以及使用2种合适的避孕方法进行避孕的情况下才能接受治疗,但如果患者已行输卵管结扎术或选择使用T型铜380AIUD或LNg20IUS进行避孕,则不需要采取另外的避孕措施。接受本药治疗的育龄期女性应该每月进行妊娠测试。
3.已存在肝脏损害
目前尚无关于已存在的肝损害对安立生坦药代动力学影响的研究。因为体内和体外证据都表明,安立生坦的清除很大程度上依赖肝脏代谢和胆汁排泄,因此肝脏损害预计会对安立生坦的药代动力学产生明显的影响。不建议中度或重度肝功能损害患者使用凡瑞克。目前没有关于凡瑞克在已有轻度肝功能损害的患者中应用的资料;然而,在此类患者中安立生坦的暴露量可能会升高。
4.肝转氨酶升高
其它内皮素受体拮抗剂(ERAs)与转氨酶(AST,ALT)升高、肝毒性和肝衰竭病例相关。对于开始服用凡瑞克后发生肝损伤的患者,应全面调查其肝损伤的诱因。如转氨酶升高>5x ULN 或转氨酶升高还伴随胆红素>2x ULN,或伴有肝功能不全的症状或体征,并且可排除其他原因,则停用凡瑞克。
5.与环孢素A合用
与环孢素A 合用时,凡瑞克的剂量应控制在 5 mg 每日一次以内。
【不良反应】
临床试验经验
凡瑞克的安全性数据来自两项在肺动脉高压患者中开展的为期12周的安慰剂对照研究(ARIES-1和ARIES-2)、以及四项在483名肺动脉高压患者(每日一次服用剂量分别为1、2.5、5、或10mg)中开展的安慰剂对照研究。在这些研究中,受试者与凡瑞克接触的时间为1天到4年不等(N=418接触至少6个月,N=343接触至少1年)。
在ARIES-1和ARIES-2中,总共261名患者每日一次服用剂量分别为2.5、5、或10mg的凡瑞克,而132名患者服用安慰剂。在接受凡瑞克治疗的患者中不良事件发生率>3%,明显高于安慰剂组(见下表)。
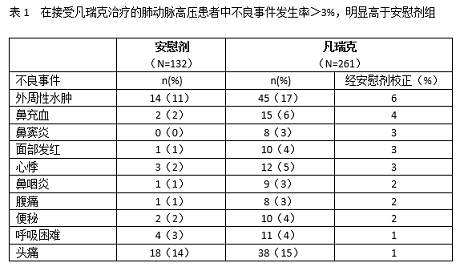
注意:这个表格包括了所有在本药治疗组中发生率>3%并且高于安慰剂组的不良事件,而且这些事件在本药治疗组和安慰剂组中发生率的差别≥1%。
大多数药物不良反应为轻至中度,仅有鼻充血呈剂量依赖性。与安慰剂组相比,本药治疗组中仅有少数患者发生的不良事件与肝功能检测有关。
仅有少数几种药物不良反应的发生率在不同年龄和性别的患者中发生率有显著差异。年轻患者中(<65岁),本药治疗组的外周性水肿发生率(14% ;29/205例)和安慰剂组(13% ;13/104例)相近 ;而在老年患者中(>65岁),本药治疗组(29% ;16/56例)的外周性水肿发生率高于安慰剂组(4% ;1/28例)。此类亚组分析的结果必需进行谨慎的解释。
在肺动脉高压患者参加临床试验的过程中,本药治疗组因为不良事件(与肺动脉高压不相关)而中断治疗的发生率(2% ;5/261例)与安慰剂(2% ;3/132例)相近。在肺动脉高压患者参加临床试验的过程中,本药治疗组中严重不良事件(与肺动脉高压不相关)的发生率(5% ;13/261例)与安慰剂组(7% ;9/132例)相近。
上市后经验
下述不良反应是在凡瑞克获得批准上市后的临床使用过程中发现的:肝转氨酶升高(常见)、肝损伤、自身免疫性肝炎,液体潴留(见【注意事项】部分),心衰(与液体潴留相关),超敏反应(如血管性水肿、皮疹、瘙痒),贫血(需要输血),眩晕, 呼吸困难,恶心、呕吐,以及虚弱、疲劳,低血压。
上市后已有报告需输注血细胞的贫血病例。10 mg 凡瑞克剂量下,血红蛋白降低(贫血)的发生频率较高。在为期 12 周的安慰剂对照III 期临床研究中,凡瑞克组患者的平均血红蛋白浓度降低,且早在第 4 周便检出(降低0.83 g/dL),在随后 8 周内较基线的平均改变量似乎保持稳定。凡瑞克组共 17 例患者(6.5%)的血红蛋白较基线降幅≥15%,且低于正常值下限。
在使用凡瑞克治疗过程中,有报道发生自身免疫性肝炎(包括自身免疫性肝炎加重)和原因不明的肝损伤。但这种不良反应发生的概率尚未知。
因为这些自发报告的反应来自规模大小不确定的人群,因此不可能估算出非常可靠的发生率、或确定一个与药物接触相关的因果关系。
【禁忌】
1.妊娠分级 X
在妊娠妇女中应用凡瑞克可能会导致胎儿损害。安立生坦口服剂量分别在大鼠≥15 mg/kg/day,以及在兔子≥7 mg/kg/day时有致畸作用;目前没有关于更低剂量的研究。在两个种属动物中都可以观察到下颚、硬腭和软腭、以及心脏和大血管的畸形,以及胸腺和甲状腺的形成障碍。致畸性是内皮素受体拮抗剂的一类作用。目前没有关于在妊娠妇女中应用凡瑞克的数据。
凡瑞克禁用于确实或可能已经怀孕的妇女。如果在妊娠期间应用该药,或在应用该药的过程中怀孕,患者应该被告知可能会对胎儿产生的危害。
对于有生育能力的女性,在开始治疗前必须排除妊娠,并且在治疗过程中以及治疗后1 个月内都应该使用两种合适的避孕方法进行避孕,但如果患者已行输卵管结扎术或选择使用T 型铜380AIUD或LNg 20 IUS 进行避孕,则不需要采取另外的避孕措施。并建议用药期间,每个月复查妊娠试验,直至停止治疗后4周。
特发性肺纤维化(IPF)
特发性肺纤维化(IPF)伴或不伴继发性肺动脉高压患者禁用安立生坦。
重度肝功能损害
对安立生坦、大豆或安立生坦片中任何一种辅料过敏者禁用。
【注意事项】
本品应由有治疗肺动脉高压丰富经验的医生决定是否开始本药治疗,并对治疗过程进行严格监测。处方本品之前应当阅读本品的医学信息手册,并告知患者服用本品的注意事项。开始本品治疗之前,患者应当先阅读本品的医学信息手册(给患者部分)。
尚未在足够数量的患者中进行研究以权衡本品治疗 WHO I 级肺动脉高压的获益和风险。尚未在WHO IV 级肺动脉高压患者中确定本品作为单药治疗的疗效。
育龄妇女:在开始治疗前必须排除妊娠。首次使用本品治疗前以及治疗期间每月进行妊娠检测。在发药前确认是否完成了妊娠检测。如在服用本品期间或停药后30 天内怀孕,与处方医师联系。
潜在的肝脏损害
应用内皮素受体拮抗剂(ERAs)可见肝酶升高。因此在开始凡瑞克治疗前应监测肝功能。如果转氨酶(谷丙转氨酶,ALT 或谷草转氨酶,AST)大于正常值上限的3 倍,则不推荐使用凡瑞克。
另外推荐每月进行肝功能监测。如果患者出现临床显著的转氨酶升高或者出现转氨酶升高并伴随其他肝损伤的体征或症状(如黄疸),则应立刻停止凡瑞克治疗。
如果患者无肝损伤或黄疸症状,在肝酶异常消退之后,可考虑重新使用凡瑞克。
已知肺动脉高压(PAH)患者会发生肝损伤和自身免疫性肝炎,特发性肺动脉高压(IPAH)患者经常产生自身抗体。已报告多例使用凡瑞克时发生了自身免疫性肝炎(包括可能的基础自身免疫性肝炎加重)和肝损伤,尚不清楚凡瑞克在这些事件中的作用。
因此,当单独使用凡瑞克或与其他已知与肝损伤有关的药品合用时,应监测肝损伤的症状并慎重使用,因为尚不清楚凡瑞克与这些药物是否有叠加效应。肺动脉高压(PAH)患者在开始凡瑞克治疗前和治疗过程中,应优化其自身免疫性肝炎的管理。如果患者出现肝炎体征或症状,或者已有自身免疫性肝炎恶化,应停用凡瑞克。
血液学改变
在应用内皮素受体拮抗剂(包括凡瑞克)后曾观察到血红蛋白浓度及红细胞压积下降,也有一些导致贫血,有时需要输血的情况出现。这些指标的下降出现在开始凡瑞克治疗后的前几周,之后则保持稳定。在为期 12 周的安慰剂对照研究中,接受凡瑞克治疗的患者在治疗结束时的血红蛋白与基线时相比平均下降 0.8g/dL。在 3 期关键临床研究的长期开放延长研究,为期4 年凡瑞克治疗期间,血红蛋白浓度与基线时相比平均下降 0.9 ~ 1.2 g/dL。
有7%接受凡瑞克治疗的患者(其中 10%的患者每日剂量为 10mg)出现血红蛋白明显下降(与基线相比降低幅度>15%,并且绝对值低于正常值低限),而与之相比安慰剂组仅有4%的患者发生此类情况。目前尚不清楚导致血红蛋白下降的原因,但它似乎不是由于出血或溶血所致。
应在开始凡瑞克治疗前、开始治疗后第 1 个月、以及随后定期检测血红蛋白。
如果患者伴有临床意义的贫血,则不推荐使用凡瑞克治疗。如果患者在治疗过程中出现有临床意义的贫血、并且排除了其它诱因,则应考虑停止凡瑞克治疗。
液体潴留
外周性水肿是内皮素受体拮抗剂类药物的一种已知效应,同时它也是肺动脉高压和肺动脉高压恶化的临床结果。在安慰剂对照研究中,与安慰剂组相比,接受5 或10mg 凡瑞克治疗的患者外周性水肿的发生率更高(见【不良反应】部分)。大部分水肿的严重性为轻至中度,且在老年患者中的发生率和严重度更高。
此外,目前已有关于肺动脉高压患者在使用凡瑞克治疗后的几周内发生液体潴留的上市后报告。患者需要使用利尿剂、限制液体摄入,或者,在某些情况下还因为心功能衰竭失代偿而需要住院治疗。如果患者之前出现过体液超负荷,则应在使用凡瑞克之前进行适当的临床处理。
如果有临床意义的液体潴留进一步发展(伴或不伴体重增加),应该开展进一步的评估以明确病因(如凡瑞克或潜在心衰),在必要的时候进行特殊治疗或中断凡瑞克治疗。
精子计数下降
为期6个月的另一种内皮素受体拮抗剂(波生坦)研究评估了药物对睾丸功能的影响,受试者为25名患有WHO功能Ⅲ级和Ⅳ级肺动脉高压并且基线精子计数正常的男性患者。使用波生坦治疗3或6个月后,有25%的患者精子计数下降了至少50%。其中一名患者在3个月时发生了明显的精子减少,并且在随后6周的2次随访中所检测的精子计数仍然很低。停止波生坦治疗后两个月,精子计数恢复到基线水平。在22名完成6个月治疗的患者中,精子计数维持在正常范围内,并且没有观察到精子形态、精子活动力、或者激素水平的变化。根据这些关于内皮素受体拮抗剂的发现和临床前数据,不能排除如凡瑞克类的内皮素受体拮抗剂会对精子发生产生不良效应。
肺静脉闭塞性疾病
如果患者在接受血管扩张药(如内皮素受体拮抗剂)治疗的初始阶段出现急性肺水肿,则应考虑肺静脉闭塞性疾病的可能性,如确诊,应停用本品。
辅料:
安立生坦片含有一水乳糖,有罕见的半乳糖耐受遗传问题,乳糖酵素缺乏或葡萄糖-半乳糖吸收障碍的患者不要服用此药;安立生坦片含有阿洛拉红铝色淀(E129),其可能导致过敏反应。
