介绍
2,6-二溴喹柄-4-氯亚胺(2,6-dibromoquinone-4-chloroimide,DBQ)是一种典型的π-电子受体,其分子结构中兼具醌式共轭骨架与溴、氯等强电子吸电子取代基,具有极强的电子接受能力。作为重要的有机π-受体,DBQ能与各类电子供体发生电荷转移(CT)相互作用形成复合物。

图一 2,6-二溴喹柄-4-氯亚胺
与哌啶的CT复合物
以氯仿为溶剂,将等摩尔的哌啶与2,6-二溴喹柄-4-氯亚胺在室温下搅拌反应 15 分钟,缓慢蒸发溶剂后得到粘稠棕色的 [(Pip)(DBQ)] CT 复合物。UV-Vis 光谱显示复合物在 399 nm 处出现特征 CT 吸收峰,对应 CT 跃迁能为 3.12 eV;IR 光谱中观察到氢键相关的特征吸收带(2626 cm⁻¹、2513 cm⁻¹、2414 cm⁻¹),证实哌啶的 - NH 基团与 DBQ 的羰基氧之间形成了分子间氢键,电荷转移通过n-π*跃迁实现。此外,采用改进的 Benesi-Hildebrand 法计算得出复合物的缔合常数(K=12.43×104 mol-1),摩尔消光系数ε=0.45×10^4 L·mol-1·cm-1,高缔合常数表明 [(Pip)(DBQ)] 复合物具有良好的稳定性[1]。
与巴比妥的CT复合物
巴比妥(Bar)作为具有镇静催眠活性的药物,是典型的电子供体。研究者以甲醇为溶剂,将 Bar 与2,6-二溴喹柄-4-氯亚胺在 60℃下加热反应 15 分钟并持续搅拌 45 分钟,室温静置 24 小时后析出暗红色的 (Bar–DBQ) CT 复合物,经表征确定其化学计量比为 1:1。红外光谱中 DBQ 的羰基振动峰从 1686 cm⁻¹ 偏移至 1620 cm⁻¹,证实羰基参与了氢键形成;¹H NMR 谱中 Bar 的 NH 质子化学位移移至 11.31 ppm,体现了复合物形成后的电子云屏蔽效应;分子对接结果显示,(Bar–DBQ) 复合物与血清素受体的结合能达 - 7.5 kcal/mol,显著高于 Bar 单体(-5.3 kcal/mol),表明 DBQ 的引入增强了巴比妥与神经受体的结合能力。
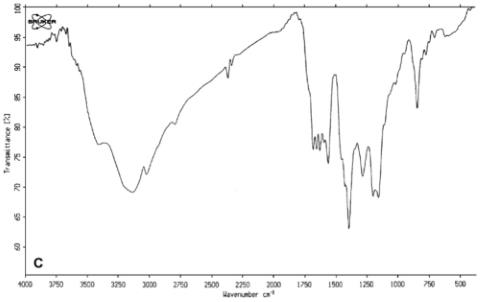
图二 2,6-二溴喹柄-4-氯亚胺的FTIR光谱
作用机制
2,6-二溴喹柄-4-氯亚胺与电子供体形成 CT 复合物的核心机制为电荷转移与氢键协同作用。一方面,DBQ的醌式 π 体系接受来自供体的孤对电子,发生从供体 HOMO到 DBQ LUMO 的电荷转移,形成特征性的 CT 吸收带;另一方面,供体的活性氢与 DBQ 的羰基氧或酰亚胺氮之间形成分子间氢键,进一步稳定复合物结构。Bar–DBQ复合物的分子静电势(MEP)图中,DBQ 的溴、氯取代基区域呈现强电负性,与巴比妥的 NH 质子的正电区域形成氢键相互作用,而电荷转移则主要发生在巴比妥的脲基共轭体系与 DBQ 的醌环之间。
哌啶-2,6-二溴喹柄-4-氯亚胺复合物在甲酸溶液中与对甲苯亚磺酸钠反应生成砜类化合物,表明复合物存在烷基 - 氧键断裂的电荷转移路径;巴比妥 - DBQ 复合物的紫外-可见光谱中,CT峰的摩尔消光系数与缔合常数的相关性,反映了电荷转移程度与复合物稳定性的正相关关系[2]。
参考文献
[1] Refat M S, Didamony H A, Abou El-Nour K M, 等. Charge-transfer interactions between piperidine as donor with different σ- and π-acceptors: Synthesis and spectroscopic characterization [J]. Arabian Journal of Chemistry, 2011, 4:105-114.
[2]S. A A ,Majid A ,F. W A , et al.Spectroscopic and Molecular Docking Analysis of π-Acceptor Complexes with the Drug Barbital[J].Applied Sciences,2022,12(19):10130-10130.DOI:10.3390/APP121910130.
