7782-44-7
中文名称
氧
英文名称
Oxygen
CAS
7782-44-7
EINECS 编号
231-956-9
分子式
O2
MDL 编号
MFCD00011434
分子量
32
MOL 文件
7782-44-7.mol
更新日期
2026/05/20 09:35:00
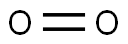 7782-44-7 结构式
7782-44-7 结构式
物理化学性质
外观性质无色无臭气体。
外观性状无色透明、无臭、无味的气体。 不易溶于水,微溶于醇。
溶解性溶于水、乙醇。
熔点−218 °C(lit.)
沸点−183 °C(lit.)
密度1.429(0℃)
蒸气密度1.11 (vs air)
蒸气压>760 mmHg at 20 °C
储存条件-20°C
溶解度At 20 °C and at a pressure of 101 kPa, 1 volume dissolves in about 32 volumes of water.
形态无色气体
颜色无色气体、液体或六方晶体
气味 (Odor)无味气体
生物来源rabbit
水溶解性one vol gas dissolves in 32 volumes H2O (20°C), in 7 volumes alcohol (20°C); soluble other organic liq, usually higher solubility than in H2O [MER06]
电导率0.02658 W/(m·K)
Merck13,7033
Dielectric constant1.5(-193℃)
介电常数1.5(-193℃)
稳定性稳定的。易燃。与磷、有机材料、许多金属粉末不相容。
化妆品成分功效SKIN CONDITIONING
InChI1S/O2/c1-2/i1+0,2+0
InChIKeyMYMOFIZGZYHOMD-ZCWHFVSRSA-N
SMILES[16O]=[16O]
表面张力15.85 mN/m at 80.0K
NIST化学物质信息Oxygen(7782-44-7)
EPA化学物质信息Oxygen(7782-44-7)
安全数据
警示词危险
危险性描述H270-H280
危险品标志O,C
危险类别码R8-R52/53-R34
危险品运输编号UN 1072 2.2
WGK Germany-
RTECS号RS2060000
TSCATSCA listed
危险等级2.2
存储类别2A - Gases
危险性类别Ox. Gas 1
Press. Gas Compr. Gas
Press. Gas Compr. Gas
应用领域
用途一
用于制液氧炸药、金属切割和焊接等用途二
用于金属的切割和焊接、炼钢,用于医疗、国防、电子、化工、冶金等行业用途三
用于光导纤维制备、电真空研究,还可用于半导体器件制备、工艺中热氧化、外延扩散、化学气相沉积等用途四
用于医院抢救病人和临床治疗用途五
包装用气体。用途六
用于金属焊接和切割。与乙炔混合可获得极高的火焰温度使金属熔融,广泛用于熔炼和顶吹氧炼钢。与水蒸气混合可用以代替空气吹入煤气气化炉内,得到较高热值的煤气。医疗上用于氧化疗法,以治疗肺炎、煤气中毒症等。化学工业用于强化硝酸和硫酸的生产。液态氧可用作液氧炸药和火箭推进剂燃剂。用途七
用于金属的切割和焊接,炼钢,医疗,国防,电子,化工,冶金等部门。参考质量标准
国家标准GB 3863—83▼
▲
指标名称
指标
I类
Ⅱ类
一级
二级
氧/%≥
99.5
99.5
99.2
水分:游离水/(ml/瓶)≤
-
100
-
露点/℃≤
-43
-
-
国家标准GB 8982—88
▼
▲
指标名称
指标
医用级
氧(体积含量)/%≥
99.5
水分(20℃,101.3 kPa)/(g/m3)≤
0.07
二氧化碳(体积含量)/%≤
0.01
一氧化碳
按GB 8986的第5章检验应合格
气态酸和碱
按GB 8986的第6章检验应合格
臭氧及其他气态氧化物
按GB 8986的第7章检验应合格
气味
无
高纯氧国家标准GB
T 14599—93
指标名称
指标
氧(V/V)/10-2≥
99.995
氩(V/V)/10-6≤
10
氮(V/V)/10-6≤
20
二氧化碳(V/V)/10-6≤
1
总碳(以甲烷计,V/V)/10-6≤
2
水分露点℃≤
-69
(10-6)
(3)
医用氧国家标准GB 8982—88
▼
▲
指标名称
指标
氧(V/V)/%≥
99.5
水分(20℃,101.3 kPa)/(g/m3)≤
0.07
二氧化碳(V/V)/%≤
0.01
一氧化碳
未检出
气态酸和碱
未检出
臭氧及其他气态氧化物
未检出
气味
无气味
制备方法
方法一
空分法首先清除灰尘和机械杂质后的空气,在压缩机中压缩。清除压缩空气中二氧化碳。干燥压缩空气,经液化、精馏、分离成氧和氮,氧气贮藏在氧气柜,液氧送入贮槽,压缩的氧气充填氧气瓶中。水电解法水在电解槽中通直流电,水即分解为氧及氢。此法可制得纯氢气,并副产得到氧气。
7782-44-7(安全特性,毒性,储运)
爆炸物危险特性
与有机物混合易爆储运特性
库房通风低温干燥; 与还原剂、可燃物分开存放毒性分级
低毒急性毒性
吸入-人 TCL0: 100000 PPM/14小时可燃性危险特性
助燃; 防止烫伤类别
有害气体灭火剂
雾状水、二氧化碳常见问题列表
简介
氧气(英语:Oxygen)是氧元素最常见的单质形态,在空气中按体积分数算大约占21%,在标准状况下是气体,不易溶于水,密度比空气略大,氧气的密度是1.429g/L 。不可燃,可助燃。
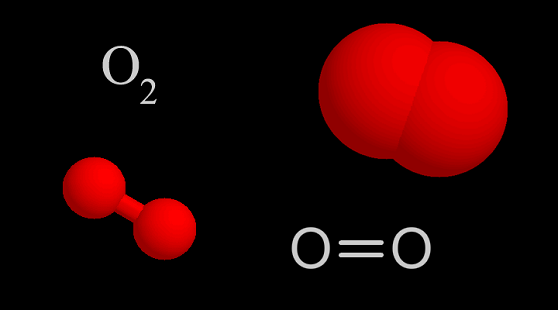
分子结构
氧气由氧分子(O2)构成。每一个氧气分子由2个氧原子构成。 氧气是双原子分子,两个氧原子形成共价键,一个2p轨道形成σ键,另两个2p轨道形成π键。其分子轨域式为(σ1s)2(σ1s*)2(σ2s)2(σ2s*)2(σ2p)2(π2p)4(π2p*)2,因此氧气是奇电子分子,具有顺磁性。
发现历史
氧气最先是由卡尔·威廉·舍勒发现的,约瑟夫·普利斯特里也于之后成功发现,但由于约瑟夫首先发表论文,所以很多人仍然认为氧气是约瑟夫首先发现的。氧气的英文名是“Dioxygen”,由拉瓦锡定名于1777年,他利用氧气所进行的试验在燃烧和腐蚀的方面打败了当时流行的燃素说。
用途
氧气的运用包括钢铁的冶炼、塑料和纺织品的制造以及作为火箭推进剂与进行氧气疗法,也用来在飞机、潜艇、太空船、潜水及火灾中维持生命。
实验室制法
实验室小规模制氧一般会加热氯酸钾和催化剂二氧化锰的混合物,生成氧气和氯化钾。其中,二氧化锰是催化剂。其发生装置是固固加热型,需要使用试管。
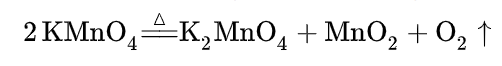
用此方法制得的氧气通常混有少量刺激性气味的气体氯气。
水中溶解度(g/100ml)
不同温度(℃)时每100毫升水中的溶解克数:1.52×10-2/30℃;1.17×10-2/10℃;9.4×10-3/20℃;7.8×10-3/30℃;6.2×10-3/40℃
毒性
毒性主要表现为对呼吸道、特别是对肺脏的损伤,严重时会出现水肿。最大容许浓度:氧的阈浓度(如进行氧气疗法)为25%~40%。在潜水工作中使用压缩氧气时应严格遵守特定的规定。压力的大小和停留时间的长短都要有所限制。缺氧引起窒死,而供氧过剩则引起中毒。毒性防护
防护措施
毒性主要表现为对呼吸道、特别是对肺脏的损伤,严重时会出现水肿。最大容许浓度:氧化的阈浓度(如进行氧气疗法)为25%~40%。在潜水工作中使用压缩氧气时应严格遵守特定的规定。压力的大小和停留时间的长短都要有所限制。缺氧引起窒死,而供氧过剩则引起中毒。
