紫苏醇学名4-异丙烯基-1-环己烯甲醇,有似芳樟醇和松油醇味的稠粘油液,存在于姜草油、青柠檬油、杂薰衣草油和留兰香等油中。因具有芳香味道,常被用作食用香精和添加剂的调配剂。紫苏醇作为一种治疗及预防癌症的单萜类药物,在肿瘤如卵巢肿瘤、食道癌、乳腺癌等的治疗方面有独到的治疗效果。
理化性质
粘稠油状液体。有似芳樟醇和松油醇气味。沸点118-121℃ (11×133.322Pa)。相对密度 0.9690。折光率1.4996 ,[α]D-7°。性质稳定, 耐热耐酸, 不易挥发。
合成方法
紫苏醇以游离态或酯的形式天然存在于柑桔、樱桃、薄荷、香柠檬、姜草、杂薰衣草等多种植物中,是植物甲醛、戊酸代谢途径产生的单萜化合物。原则上,紫苏醇可从天然植物精油中单离获得,如Row等采用有机溶剂或超临界CO2萃取提取紫苏醇。虽然紫苏醇存在于多种天然植物精油中,但因含量太低、分离不易而成本过高,因此化学合成紫苏醇就显得尤为重要。有关紫苏醇的合成,大多采用天然存在的单萜化合物为起始原料,经合适的化学转化来进行的。
1、 苧烯氧化法
苧烯是柠檬油、甜橙油、香柠檬油、莳萝油等天然精油的主要成分, 因而其来源是相当丰富的 。从分子结构看, 苧烯与紫苏醇具完全相同的分子骨架结构( 图1) , 在适当的反应条件下, 苧烯可经氧化转化生成紫苏醇。
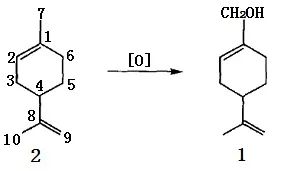
图1 苧烯的分子结构
空气或氧气对苧烯的氧化作用或催化氧化曾有广泛的研究,二氧化硒也可对其进行选择性氧化。但由于苧烯氧化合成紫苏醇是对烯丙位的甲基氢进行氧化,而苧烯分子中有5种不同的烯丙位的氢(如图1所示的3、4、6、7和10位上的氢),因而通常氧化反应的产物十分复杂,紫苏醇的选择率很低。
2、β-蒎烯直接氧化法
Willing等在含有氯化亚铜、苯甲酸铜的乙腈中用过氧化二苯甲酰氧化β-蒎烯,获得主要产物反式香芹醇(产率29.4%)和少量的紫苏醇。夏克坚等采用同样的方法进行β-蒎烯的氧化反应,紫苏醇产率为73%。南京林业大学程芝等用四乙酸铅作氧化剂,β-蒎烯经氧化或氧化酯化、皂化制得紫苏醇,优化条件下紫苏醇收率可达45%。直接氧化法所得紫苏醇产率太低,且产物十分复杂,难以分离提纯,因此应用价值不大。
3、以α-蒎烯为原料合成
以α-蒎烯为原料(4)合成紫苏醇有2种方法,其一是以二氧化硒SeO2为氧化剂在醋酸-醋酐混合溶剂中发生烯丙位选择氧化或氧化-酯化反应,生成桃金娘烯醇(5a)及其乙酸酯(5b),再经异构化、皂化即得1。
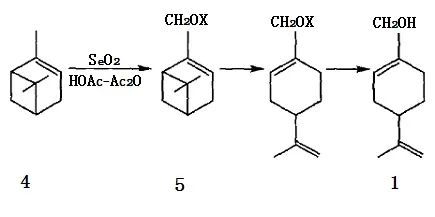
图2 α-蒎烯用SeO2 氧化合成紫苏醇
4、β-蒎烯环氧化物重排法
Bluthe等利用β-蒎烯环氧化物(6)在汞离子存在下与水作用,首先生成二醇,再在稀硫酸催化下脱水后可定量地转化成紫苏醇;这一方法在Sy-narome等的一份专利中也有报导,据称紫苏醇的得率可达98%,但反应中硫酸汞的用量几乎是环氧蒎烷的一倍,实为不足之处。β-蒎烯环氧化物在酯酸钠存在下与羧酸RCOOH(R=H、Me、Et、tPr)反应可转化成醇和相应酯的混合物,经水解可制得紫苏醇。2,10-环氧蒎烷的酸催化异构化是综合利用我国资源丰富的松节油中的β-蒎烯来合成紫苏醇的最有效的途径,由于2,10-环氧蒎烷可以很方便地由β-蒎烯经环氧化反应制备,这也为β-蒎烯资源的综合利用提供了一条新途径(图3)。
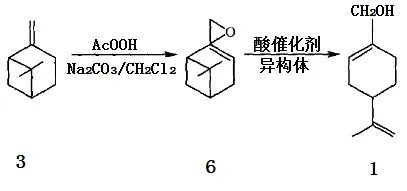
图3 2, 10-环氧蒎烷在酸催化下的异构化反应
5、紫苏醇的生物转化
(1)、含CYP153A6的重组微生物细胞区域选择性羟基化(S)-柠檬烯为(S)-紫苏醇[1]
细胞生理是决定微生物生物催化剂反应效率的关键因素。为探索细胞色素P450单加氧酶CYP153A6重组恶臭假单胞菌细胞将(S)-柠檬烯羟基化转化为(S)-紫苏醇的有效工艺条件,对其生理参数进行了优化。之前报道的putida GPo12合成(S)-紫苏醇的方法是基于复杂而敏感的辛烷摄食策略,表明了细胞生理学的关键作用。与之前的研究结果相比,对不同碳源的筛选表明,甘油和柠檬酸是辛烷的合适替代品,具有较高的柠檬烯羟基化活性。putida KT2440作为替代宿主菌株和柠檬酸盐作为碳源改善了实际处理,并允许比活性增加7.5倍(22.6 U gCDW -1)。在两液相生物转化中,在24小时内生产了4.3 g (S)-紫苏醇Ltot (-1),与以前报道的结果相比,生产率提高了6倍。因此,在活微生物细胞中选择性细胞色素p450烃类氧化功能化过程中,细胞生理与目标生物转化之间的关系至关重要,了解这一关系可以指导生物催化剂和生物过程的设计。
在本研究中,Cornelissen等详细研究了是哪些生理参数限制了含CYP153A6的整个假单胞菌细胞催化(S)-柠檬烯羟基化为(S)-紫苏醇(图4),目的是开发一种高效的生物转化过程。
虽然基于细胞色素细胞的生物氧化具有很高的工业应用潜力,但所取得的生产力往往太低,不具有经济意义。在两液相生物转化中,(S)-柠檬烯转化为(S)-紫苏醇受细胞生理限制,而不受CYP153A6固有特性的限制。谨慎的宿主和碳源选择允许休眠细胞的比活性增加7.5倍。在双液相生物转化中,优化的生理条件和过程控制转化为6倍的生产率比以前报道的结果。确定的进一步限制包括底物可用性和过度氧化。可以预见,类似的参数限制了许多其他基于CYP2的生物转化的反应效率。因此,强烈建议在设计全细胞催化剂时考虑生理效应。
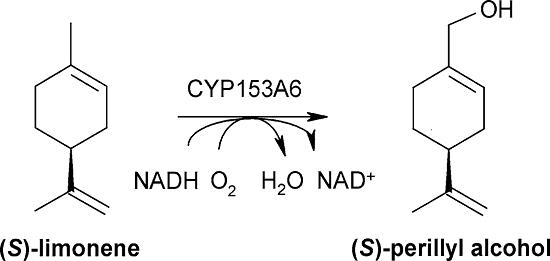
图4 紫苏醇的生物转化 [1]
(2)、重组大肠杆菌对紫苏醇生产的影响[2]
(R)-(+)-紫苏醇是一种天然含氧单萜,广泛用于天然香料添加剂、杀虫剂、喷气燃料和抗癌疗法。它也是容易获得的单萜前体。然而,这种天然产物存在于低浓度的植物来源,这在经济上是不可行的。因此,微生物生产方法正迅速成为一种有吸引力的替代方法,使(R)-(+)-紫苏醇生产更加可持续和环境友好。[2]
Sun等设计了一种外源的甲羟戊酸(MVA)途径,包括柠檬烯合成酶、对伞花烃单加氧酶羟化酶和对伞花烃单加氧酶还原酶,用于生产(R)-(+)-紫苏醇。从葡萄糖中得到(R)-(+)-紫苏醇的单萜前体(R)-(+)-柠檬烯的浓度达到45 mg/L。从而实现了(R)-(+)-紫苏醇的增强型生产。该菌株在5l的间歇式生物反应器中产生(R)-(+)-紫苏醇,滴度为87 mg/L,葡萄糖产率为1.5 mg/g。这些数据强调了通过甲戊酸途径从葡萄糖高效生产(R)-(+)-紫苏醇。该方法为今后生产其他单萜类化合物提供了参考依据。[2]
众所周知,在(S)-(−)-紫苏醇生产过程中,使用大肠杆菌可使滴度提高100 mg/L。许多萜类化合物已经通过代谢工程高效价生产,包括单萜、倍半萜、二萜和四萜。以嗜热硬脂芽孢杆菌(LHBS)的柠檬烯羟化酶为底物(R)-(+)-柠檬烯可产(R)-(+)-紫苏醇0.51 mg/L。将LHBS连接到pET28a(+)中创建pSC00,同时创建pSC01中的cymAa和cymAb。柠檬烯对大多数微生物具有毒性,其浓度可以调节BL21 (DE3)的生长。因此,评价间歇式生产加料中柠檬烯的浓度是很重要的。不同(R)-(+)-柠檬烯浓度评估(0.2 mM至3.0 mM)的生长试验。随着(R)-(+)-柠檬烯浓度的增加,细胞生长受到抑制。在(R)-(+)-柠檬烯浓度为1.0 mM时,SC01的OD600从2.5下降到2.0。当(R)-(+)-柠檬烯用量为2 mM时,SC01的产量为86.9 mg/L,紫苏醇的转化率为30%。另一株菌株SC00产生1.5 mg/L的低浓度,细胞生长受到抑制。在后续的研究中,以菌株SC01为研究基础。产物经乙酸乙酯有机萃取后经GC-MS鉴定。对照试验中大肠杆菌提取物缺乏cDNA克隆,不产生(R)-(+)-紫苏醇,而携带恶臭假单胞菌cymAa和cymAb的大肠杆菌产生的(R)-(+)-紫苏醇达到可检测量。实验结果表明以(R)-(+)-柠檬烯为底物成功构建了(R)-(+)-紫苏醇的生物合成途径。
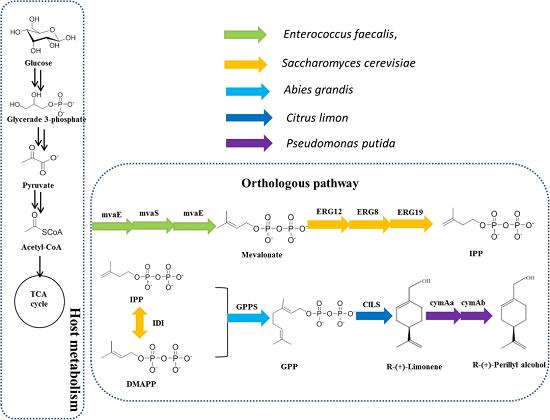
图5 通过MVA途径产生(R)-(+)-紫苏醇
