背景及概述
苯基哌嗪类化合物具有不同程度的5-HT受体阻断活性,并且将该部分与其他部分载体相结合则可以使化合物具有中枢神经调节作用或中枢及外周降压活性。(4-哌嗪-1-基)苯甲酸乙酯是苯基哌嗪类抗抑郁症药物的中间体,尤其是合成调节神经类药物如阿立哌唑的关键原料。4-(1-哌嗪基)苯甲酸乙酯英文名称:Ethyl 4-(piperazin-1-yl)benzoate,中文别名:(4-哌嗪-1-基)苯甲酸乙酯,CAS号:80518-57-6,分子式:C13H18N2O2,分子量:234.294。
制备
以二乙醇胺为起始原料,无溶剂条件下经氯代反应制得β,β′-二氯代二乙基胺盐酸盐,不经分离直接滴加取代苯胺和相转移催化剂,经环合反应合成目标化合物(4-哌嗪-1-基)苯甲酸乙酯[1]。
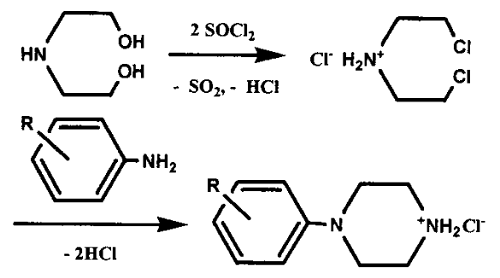
图1 (4-哌嗪-1-基)苯甲酸乙酯的合成反应式如下图
实验操作:
将52.3g(0.44mol)氯化亚砜溶于10mL氯仿,置于装有回流冷凝管和冰水浴的四口烧瓶中,机械搅拌,用水吸收尾气。缓慢滴加二乙醇胺21.5g(0.2mol)与15mL氯仿的混合液,滴加过程中控制反应液温度不超过30℃,滴加时间3h。滴加完毕后,撤去冰水浴,室温反应1h,然后缓慢升温,待固体完全溶解后升温至50℃,继续反应0.5h,停止加热,冷却至室温,抽滤,得到白色微黄绿色固体,用无水乙醇重结晶,得到白色针状晶体。将β,β′-二氯代二乙基胺盐酸盐(12.7g,0.07mol)溶于55mL水中,置于装有回流冷凝管的四口烧瓶中,机械搅拌,加热使固体完全溶解,滴加0.07mol取代苯胺,每半小时检测pH一次,滴加50%碳酸钠水溶液,使反应体系pH保持为6,最终pH不再减小,停止加热,静置冷却至室温,过滤,滤饼用水、无水乙醇各洗涤两次,烘干,得到白色晶体。
讨论
氯代反应的影响因素
氯代试剂的选择
醇的卤化反应常用的方法有:①醇与卤化磷反应;②醇与氢卤酸反应;③醇与氯化亚砜反应。方法①后处理比较麻烦,方法②必须使用高浓度强酸来促使反应并需要加入脱水剂,两个方法的产率均较低;方法③反应的副产品均为气体,很容易离开反应体系,有利于反应向产物方向进行,氯化亚砜廉价易得,反应速度快、易操作、产率高、副反应少。因此选择氯化亚砜作为氯代试剂来合成β,β′-二氯代二乙基胺盐酸盐。
反应物物质的量比对产率的影响
一种反应物过量会增大另一种反应物的转化率,从而提高产率。表4显示的是其他条件相同,仅二乙醇胺与氯化亚砜物质的量比不同条件下β,β′-二氯代二乙基胺盐酸盐的产率。二乙醇胺与氯化亚砜物质的量比为1∶2时产率为67.5%,随着氯化亚砜的增多,产率提高,物质的量比为1∶2.3时达到最高为78.7%,氯化亚砜继续增加产率下降,原因是生成的β,β′-二氯代二乙基胺盐酸盐可溶于氯化亚砜。剩余过多氯化亚砜需要延长加热时间才能除去,产生大量污染性气体,并且加热时间过长易导致β,β′-二氯代二乙基胺盐酸盐氧化变红棕色。
环合反应的影响因素
合成哌嗪反应及溶剂的选择
本文采用的方法是β,β′-二氯代二乙基胺盐酸盐与取代苯胺在水中反应并加入缚酸剂,发生环合反应生成取代苯基哌嗪盐酸盐。目标产物不溶于水,直接从水溶液中析出。简化了后处理操作,大幅度减少污染性废液量;也不需要使用催化剂,成本较低。值得注意的是反应物取代苯胺不溶于水,使两种原料处于不同的两相,分子碰撞机会减小,解决的方法是使用相转移催化剂并且加快搅拌速度打浆,试验表明,相转移催化剂(例如PEG600)并不能提高产率,只需要加快搅拌速度打浆即可。反应过程中产生氯化氢与取代苯胺结合生成的取代苯胺盐酸盐易溶于水而进入水相,这就增大了原料分子碰撞机会,使反应能够进行。β,β′-二氯代二乙基胺盐酸盐与取代苯胺反应,和第二个氯原子的取代均按SN2反应历程进行。β,β′-二氯代二乙基胺盐酸盐结构中的伯卤代烷由于卤素所处位置空间位阻较小,因而易受到氨基的亲核进攻,卤素从被进攻方向的背面离去;在质子中和剂存在的条件下,可将卤代烷与取代苯胺环合产生的氯化氢转化为水,从而使反应平衡向产物方向进行。
缚酸剂对产率的影响
部分取代苯胺与反应过程中产生的氯化氢结合而进入水相,这就增大了取代苯胺与β,β′-二氯代二乙基胺分子碰撞的机会,促进产率提高,但是大量的氯化氢会抑制反应向正方向移动,不利于产物的生成,因此需要加入缚酸剂来控制溶液中氯化氢的量。缚酸剂的种类和体系pH对苯基哌嗪盐酸盐产率的影响使用碳酸钠时产率相对较高,因此选用碳酸钠来中和氯化氢,生成的氯化钠溶于水而与产物分离。向反应体系中加入碳酸盐时,容易产生大量泡沫溢出反应器。使用强碱产率低的原因是氢氧根易于发生亲核反应。从试验结果来看,反应体系的pH保持在6时产率最高。pH大于7时只能产生少量的目标产物,这是因为在碱性条件下两种原料会出现相面分离。pH小于6时产率降低,是因为溶液中氯化氢过多而抑制反应。氯化氢量较少也便于产物形成盐酸盐从溶剂中结晶析出,因此控制反应体系pH保持在6为宜。
结论
以二乙醇胺为起始原料,无溶剂条件下经氯代反应制得β,β′-二氯代二乙基胺盐酸盐,不经分离直接滴加对氨基苯甲酸乙酯和相转移催化剂,经环合反应合成目标化合物(4-哌嗪-1-基)苯甲酸乙酯。产率48.3%,纯度95.7%。讨论了各步反应的影响因素。产物经红外光谱、核磁共振氢谱分析验证与目标化合物的结构一致。该方法经济环保,省时,易操作。
参考文献
[1] Ey al M, Carmen S D, Timothy J M .Formation of pheny-lpiperazines by a novel Alumina supported bis-alky lation [ J] .Tetrahedron Letters, 1996, 37 ( 3) :319-322.
