背景及概述
2-氯-6-三氟甲氧基苯并噻唑及其衍生物是一类非常重要的杂环化合物,普遍存在于大自然中,主要应用于医药、农业及工业等领域。近年来,随着越来越多合成苯并噻唑类衍生物的方法被研究出来,其制备方法受到了广泛的关注。由于2-氯-6-三氟甲氧基苯并噻唑具有良好的药理活性和生物活性,其制备方法受到了广泛的关注。
制备
制备苯并噻唑类衍生物的方法非常之多。以前主要以邻氨基苯硫酚与醛、羧酸、腈类、酯类等缩合生成苯并噻唑类衍生物,也可以由硫代酰胺或硫脲的环合反应来制备。由于硫脲或硫代酰胺这类化合物的制备路线长,合成成本昂贵;而邻氨基苯硫酚不稳定,容易被氧化成二硫化物。所以,近年来又发现了以稳定易得的芳香邻氨基二硫化物或者以邻卤苯胺为原料来合成苯并噻唑类化合物的新方法,此外还有一些其它原料合成苯并噻唑类衍生物的方法。氨基苯硫酚是目前制备苯并噻唑类化合物的常用原料,它可以与醛、羧酸、腈类、酯类等缩合生成苯并噻唑类化合物。本文以利鲁唑为原料,与硫酸肼回流反应将其2-位氨基转化为肼基制得2-肼基-6-三氟甲氧基苯并噻唑;经氯化亚砜氯代制得2-氯-6-三氟甲氧基苯并噻唑[1]。苯并噻唑的合成反应式如下图:
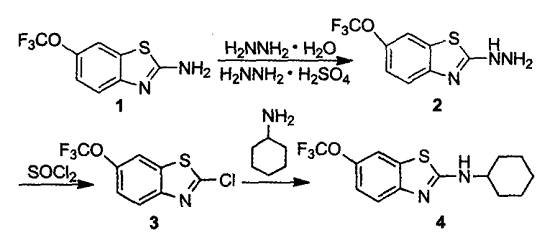
图1 2-氯-6-三氟甲氧基苯并噻唑的合成反应式
实验操作
方法一、
向50mL平行合成仪反应管中依次加入0.4mmol的2,2’-二硫代二苯胺、0.80mmol的芳香醛、0.2mmol的而硫化钠和0.2mmol的碳酸氢钠,放入磁子,在氮气保护下,再加入3mL的N,N-二甲基甲酰胺作为反应溶剂,在100℃下搅拌反应,采用薄层色谱监测反应。当反应5-8h后,停止反应,冷却至室温。反应液用二氯甲烷和亚硫酸氢钠溶液萃取,收集有机相。再向有机相中加入无水硫酸钠干燥30min,过滤除去无水硫酸钠后,减压蒸馏除去二氯甲烷,得到粗产物。粗产物用石油醚和乙酸乙酯作展开剂,进行柱层析分离(200-300目硅胶)后,得到了2-氯-6-三氟甲氧基苯并噻唑。
方法二、
2-肼基-6-三氟甲氧基苯并噻唑的合成
在500mL三口瓶中依次加入乙二醇350mL,利鲁唑23.42g(0.1mol),硫酸肼19.52g(0.15mol)和82%水合肼80mL,氮气保护下升温至135℃,搅拌下回流反应4h(TLC监测)。冷却至室温(析出大量白色晶体),加适量冷水,搅拌使其沉淀完全,抽滤,滤饼用冷水洗涤,真空干燥得鱼鳞状灰白色晶体18.7g的2-肼基-6-三氟甲氧基苯并噻唑。
2-氯-6-三氟甲氧基苯并噻唑的合成
在三口瓶中加人氯化亚砜120mL,加冷凝管和尾气吸收装置,升温至65℃,搅拌下缓慢加入2-肼基-6-三氟甲氧基苯并噻唑12.45g(0.05mol),滴毕(约1.5h),于60℃反应4h。减压蒸出氯化亚砜,残余物用适量二氯甲烷溶解,减压蒸出溶剂,重复该操作4~5次,直至残余氯化亚砜被除净。残余物用适量二氯甲烷溶解,依次用水洗涤、无水硫酸钠干燥,蒸除溶剂,冷却得淡红褐色固体,用石油醚(60~90℃)重结晶得白色晶体310.71g,即2-氯-6-三氟甲氧基苯并噻唑。
结果与讨论
2-肼基-6-三氟甲氧基苯并噻唑的稳定性较差,因此反应中需氮气保护,产物需要真空干燥。反应液中加等体积水以使2-肼基-6-三氟甲氧基苯并噻唑沉淀完全,本实验发现加水会导致收率降低。本文采用低温的方法,反应液冷却至室温后,加适量冰水,收率较高,并且纯度好,不需分离提纯,真空干燥后直接使用。
在2-氯-6-三氟甲氧基苯并噻唑的合成中反应产生二氧化硫,需要尾气吸收装置。该反应较快,产生大量气体,应缓慢分批加入反应物。产物熔点较低,除去溶剂后残余物为褐色油状,冷却后呈固态。用二氯甲烷反复蒸馏,以完全除掉氯化亚砜,而实际上氯化亚砜仍有残留。因此需要将产品溶于二氯甲烷后,用水反复洗涤。
参考文献
[1] Saha P,Ramana T ,Purkait N ,et a1.Ligand free copper—catalyzed synthesis of substituted benzimidazoles ,2 -aminobenzimidazoles ,2-aminobonzothiazoles ,an d benzoxazoles[J].J Org Chem ,2009,74(13):8719-8725.
