喹诺酮类(quinolones,QNs)药物是一大类具有1,4-二氢-4-氧代喹啉-3-羧酸结构的人工合成抗菌药物, 1962年由Lesher等研制而成,代为萘啶酸,自发明后1963年应用于临床。后30年迅速发展,其发展的速率超过了头孢菌素类(3.0%)及青霉素类(4.1%)抗菌药物。其抗菌谱广、抗菌活力强、体内分布良好、不良反应小,且与其他药物合用不良配伍少,对多种耐药菌有较好的疗效。常被用作青霉素及头孢菌素替代药物治疗全身感染。喹诺酮类药物与细菌DNA促旋酶及拓扑酶发生交互作用,导致DNA发生降解或菌体死亡。因此,喹诺酮类药物在抗菌药物中占有重要地位。
喹诺酮类属化学合成药,按其发明先后及其抗菌性能的不同,分为四代:
代萘啶酸抗菌谱窄,仅对部分菌株有抗菌作用,对葡萄球菌属、铜绿假单胞菌等均无抗菌作用,目前临床已不使用。
第二代吡哌酸是国内主要应用品种,抗菌活性强,对铜绿假单胞菌抗菌活性强,不良反应较萘啶酸少,用于尿路与肠道感染。
第三代对铜绿假单胞菌有较好的抗菌作用,对革兰阳性球菌也有一定抗菌作用,广泛用于泌尿生殖系统、胃肠道疾病,以及呼吸道、皮肤组织的革兰阴性细菌感染的治疗,常用的有诺氟沙星、氧氟沙星、环丙沙星、依诺沙星、左氧氟沙星、洛美沙星、氟罗沙星、培氟沙星、帕珠沙星。
第四代抗菌谱是目前为止的,对大部分厌氧菌,革兰阳性菌的耐菌寄铜绿假单胞菌的抗菌活性也明显提高。例如克林沙星、加替沙星、莫西沙星、司帕沙星。
【药品概况】[2]
通用名称:喹诺酮
英文名称:Quinolones
结构式:喹诺酮类药物母核主要有两种结构:一种是分别在1- 位和8- 位是氮原子的二并吡啶核,称为萘啶酸核;另一种就只含有一个氮(在1- 位)的核,这样的核则称为喹诺酮核。
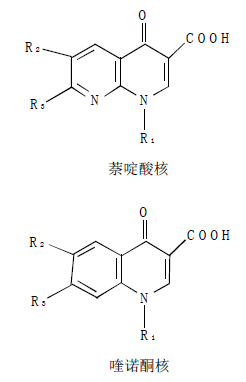
图1为喹诺酮类药物母核主要有两种结构
【适应症】
诺氟沙星:对革兰阴性菌抗菌力较强,尤其对大肠埃希菌、铜绿假单胞菌、奇异变形菌、淋菌等有较好抗菌作用。对耐药金黄色葡萄球菌也有较好作用,对庆大霉素、头孢氨苄和甲氧苄啶等耐药的菌株仍有良好抗菌作用。主要用于泌尿道、呼吸道及妇科、外科、
皮肤科等感染。
依诺沙星:本药抗菌活性强,优于诺氟沙星,对葡萄球菌属、链球菌属、大肠埃希菌、克雷伯菌属、铜绿假单胞菌、变形菌属、及其他假单胞菌、流感菌属等有良好的抗菌作用。主要用于敏感菌所致的支气管、肺、尿道、肠道、胆囊、中耳等部位的感染。成人常用量300~600mg/d,分3次服。
氧氟沙星:对葡萄球菌属、肺炎链球菌、其他链球菌、大肠埃希菌、志贺菌属、淋菌、流感嗜血菌、变形菌属、柠檬酸杆菌属、支原体属、不动杆菌属等有较好的抗菌作用;还有抗结核作用,它与抗菌药物无交叉耐药,对厌氧杆菌活性优于诺氟沙星2~16倍。主要用于呼吸道、扁桃体、咽部、泌尿道、皮肤、胆管、胃肠道等感染性疾病。常规成人用量200~300mg/d。
左氧氟沙星:具有广谱抗菌作用,抗菌作用强,对多数肠杆菌科细菌,如大肠埃希菌、克雷伯菌属、变形菌属、沙门菌属等革兰阴性菌有较强的抗菌活性;对金黄色葡萄球菌、肺炎链球菌、酿脓链球菌等革兰阳性菌和肺炎支原体、衣原体也有抗菌作用。主要用于泌尿系、呼吸系统、胃肠道、骨和关节、皮肤感染。
环丙沙星:是喹诺酮类抗菌活性较强的一种抗菌药,对革兰阳性球菌抗菌性较其他同类抗菌药强,对大肠埃希菌、流感菌属、链球菌属、金黄色葡萄球菌优于同类药物,且耐药性低。常用语呼吸系统、泌尿系、消化道、皮肤和软组织、五官科感染。常规成人口服250mg/次。
培氟沙星:本药能够迅速进入脑脊液及骨组织,口服吸收好,主要对于敏感的革兰阴性菌及葡萄球菌属感染疗效好,对心内膜炎、细菌性脑膜炎、肾及泌尿道、妇科、呼吸道等感染有较好疗效。口服800mg/d,首次口服可用全日量迅速达到血药浓度。
洛美沙星:本药抗菌范围与氧氟沙星类似,主要范围包括葡萄球菌属、大肠埃希菌、卡他球菌、流感菌属、变形菌属,对革兰阴性杆菌体外有抗菌作用。对肺炎链球菌及支原体属、厌氧菌无效,应注意区别使用。口服吸收95.0%~98.0%,以原形尿排出。主要用于敏感菌所致的下呼吸道及泌尿道感染。
氟罗沙星:主要抗菌范围包括革兰阴性菌、如革兰阳性菌,如大肠埃希菌、淋菌、沙门菌属、金黄色葡萄球菌等,高浓度可对铜绿假单胞菌有抗菌作用;口服吸收好,主要以原形随尿液排泄。
莫西沙星:本药物对常见的呼吸道敏感菌、青霉素敏感菌、耐药肺炎链球菌、嗜血菌属、卡他莫拉菌及肺炎支原体、衣原体、军团菌较敏感,口服吸收好,22%原形尿排泄。常用于敏感菌所致的呼吸道感染,包括慢性支气管炎急性发作,或轻中度社区获得性肺炎。
【药理作用】[3]
喹诺酮抗菌药物主要通过与细菌的DNA旋转酶结合,形成DNA三联复合物,以阻止细菌DNA复制与转录,而导致细菌死亡。本类药物属杀菌剂,抗菌谱广,抗菌特点包括:
1. 对需氧革兰阴性杆菌具有强大抗菌,尤肠杆菌属作用最强。
2. 对葡萄球菌、铜绿假单胞菌、某些链球菌及支原体、衣原体有效;此外对胞内病原菌如伤寒、弓形虫、军团菌、结核分枝杆菌等具良好作用。
3. 对厌氧菌均无效。
4. 组织体液中浓度高、体内分布广。
5. 消除半衰期长,多数品种有口服及注射剂两种制剂。
【药物动力学】[4]
与早期的喹诺酮相比, 新氟喹诺酮类药物的药物动力学性质明显改善, 经胃肠道吸收迅速且几乎完全。口服给药时的Cmax 与静脉给药时几乎相等, 故在多数情况下可采用口服给药途径。此外, 只要住院患者对口服给药时的耐受性良好, 就应将静注转变为口服,以利患者及早出院并降低治疗费用。
与铝、镁、钙或锌制剂联用时, 氟喹诺酮的口服吸收明显降低, 这是因为它们在胃肠道中发生螯合作用而形成难溶性的药物-阳离子复合物。在口服氟喹诺酮前至少4h 或后至少2h 再服用这些金属离子制剂,则可基本避免对氟喹诺酮吸收的影响。由于硫糖铝中含有铝, 它也同样会降低喹诺酮的吸收, 但鉴于目前尚未确定它们之间的用药间隔, 故应避免喹诺酮与硫糖铝的联合用药。
氟喹诺酮的分布容积大, 组织分布广泛, 组织浓度一般大于其血药浓度。它们对肾、肺、前列腺、支气管、鼻、胆囊、胆汁和生殖系统组织等均具有很强的渗透性。某些氟喹诺酮, 如环丙沙星和氧氟沙星的尿药浓度是其血药浓度的25 倍, 因此, 它们特别适于泌尿道感染的治疗。
氟喹诺酮药物广泛分布于呼吸道组织和体液中,故能有效地对付常见呼吸道病原菌引起的感染。由于曲伐沙星能够通过未发炎的脑膜, 从而使它将来有可能成为治疗某些严重的细菌性脑膜炎的个喹诺酮类药物。
新氟喹诺酮的半衰期较长, 可一日1 次或一日2次给药。喹诺酮通常经肾脏和非肾脏两种途径清除。不同喹诺酮的清除途径不同, 其中, 氧氟沙星和左氧氟沙星完全经肾脏清除;萘啶酸、西诺沙星、诺氟沙星、环丙沙星、依诺沙星、洛美沙星、加替沙星、莫西沙星和司帕沙星经肾脏和非肾脏(胃肠或肝脏)共同清除。对以肾脏清除为主的氟喹诺酮必须根据肌酸酐的清除率对其用药剂量进行适当调整。
曲伐沙星主要经肝脏清除, 用药后约给药量的50 %经肝代谢;43 %以原药形式经粪便排泄。典型的肝脏疾病可能会延长曲伐沙星的消除半衰期。对轻中度肝硬化患者必须调整用药剂量。目前还没有关于重度肝病患者采用曲伐沙星疗法的公开报道。
由于老年患者或多或少存在肝功能障碍且氟喹诺酮在肝中的分布容积较小, 致其血药浓度相对较高。但不存在其它危险因素时, 仅因为患者年龄高则不必调整用药剂量。
【临床应用】
临床主要应用抗菌活性强、毒性低的氟喹诺酮第三、四代类药物。
1.泌尿生殖道感染
2.肠道感染
3.呼吸道感染
4.骨骼系统感染
5.皮肤软组织感染
6.其他 pefloxacin可治疗化脓性脑膜炎和由克雷伯菌属、肠杆菌属、沙雷菌属所致的败血症。
【不良反应】[1]
喹诺酮类药物的不良反应发生率为3.1%~16.2%。常见反应有:(1)胃肠道反应:常见为恶心、呕吐、腹痛、腹泻、厌食,此类的不良反应一般可耐受。(2)中枢神经系统反应:表现为头晕、头痛、失眠、谵妄、精神萎靡、癫痫、大多为可逆性,但有精神及癫痫者慎用或禁用。此类不良反应大多由于能够穿透血脑屏障而引发。(3)皮肤及光敏毒性:表现为皮疹、丘疹、大多与用药剂量及用药速度有关,发生率高,与剂量有较大关系。(4)肝肾毒性:国内资料报道肝功能损害居多,表现为一过性谷丙转氨酶升高,大部分资料认为与肝脏的直接作用有关系,国外报道肾损害较多,常为间质肾炎。(5)关节病变:本类药物可导致幼龄动物软骨损伤,但人类此类报道尚无,临床常为儿童禁用药。(6)血系统毒性:临床有导致白细胞数量降低,溶血贫血、再障性贫血等报道,还有部分病例出现心脏不良反应,但均为可逆性。
【药物相互作用】[5]
与本类药物有重要相互作用的药物有:
①碱性药、抗胆碱药、H2受体阻滞剂等降低胃液酸度的药物,可减少本类药物的吸收。
②抑制RNA和蛋白合成药,如利福平、氯霉素等,可使本类药品降效或失效。
③氟喹酮类抑制茶碱代谢,使后者血药浓度升高,引起中毒。
【残留检测】[6]
目前喹诺酮(QNs)的检测方法主要有高效液相色谱法(HPLC)、高效液相-串联质谱法(HPLC-MS-MS)、酶联免疫法(ELISA)、微生物法、高效毛细管电泳分析法等。酶联免疫法可能造成样品假阳性,不适合作残留确证,适用于大量样品的快速筛选;微生物法检测限过高,特异性不强;高效毛细管电泳分析法的检测限也较高;HPLC法特异性强、定量准确,缺点是测定种类少、不能作定性分析、检出限难以进一步降低HPLCMS-MS法灵敏度高、检测限低、测定种类多、集高效分离和结构鉴定于一体,该仪器在我国检测机构中的配置也较为普遍,已成为复杂混合物中痕量组分定性和定量的有力工具,国家标准中近一半方法为液质方法。
【主要参考资料】
[1] 戴丽.喹诺酮类药物临床应用及不良反应[J].中华医院感染学杂志,2012,1(22):163-164.
[2] 李雅丽等.喹诺酮类药物残留检测方法[J].食品科学,2007,11(28):628-634.
[3] 蒋晓磊等.喹诺酮类抗菌药物研究新进展[J].中国抗生素杂志,2011,4(36):255-263.
[4] 蒋锦,刘明亮.喹诺酮类抗菌药的新分类方法及合理用药[J].国外医药抗生素分册,2003,6(24):272-276.
[5] 喹诺酮类 - 新全实用药物手册 - 中国工具书网络出版总库
[6] 李佩佩等.色谱法检测动物源食品中喹诺酮类药物残留研究进展[J].食品科学,2013,3(34):303-307.
