7 月 6 日,据 Insight 数据库显示,安进「注射用卡非佐米」上市申请进入在审批阶段,预计近期即将获批,该药主要用于治疗多发性骨髓瘤。点击查询审评进度
图片来源:Insight 数据库(https://db.dxy.cn/)
卡非佐米(carfilzomib),商品名:Kyprolis,是一种蛋白酶体抑制剂,最初由 Proteolix 公司研发,2009 年由奥尼克斯(Onyx) 收购 Proteolix 获得该品种, 2012 年 7 月 20 日获 FDA 批准上市,用于至少接受过两种(硼替佐米和免疫调节剂)先前的多发性骨髓瘤患者。后又获批联合来那度胺和地塞米松治疗接受过 1-3 次先前疗法的复发多发性骨髓瘤患者。
2013 年 8 月 27 日,安进以 104 亿美元的价格收购奥尼克斯制药公司,并获得 Kyprolis 的专利权。
多发性骨髓瘤(multiple myeloma, MM)是起源于 B 细胞系的恶性肿瘤,其特征在于恶性浆细胞在骨髓微环境克隆增殖,引起骨折和骨髓功能衰竭,是全球第二个最常见的血液系统肿瘤,依靠传统的化疗方案不能够治愈。
硼替佐米(brotezomib)是个蛋白酶体抑制剂,是多发性骨髓瘤的一线用药,但是其具有较强的耐药性,卡非佐米(carfilzomib)是继硼替佐米后第二个被 FDA 批准蛋白酶体抑制剂。据安进 2019 年财报显示,Kyprolis 全球销售额为 10.65 亿美元。
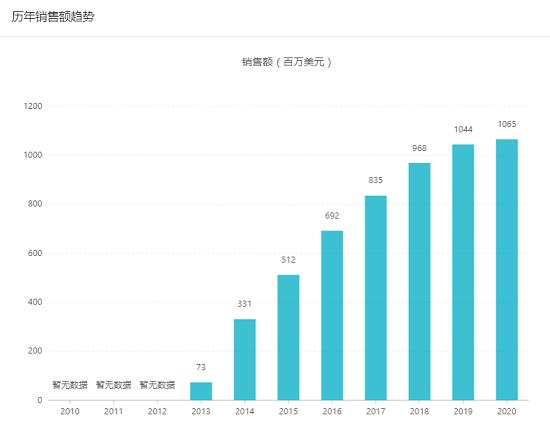
图片来源:Insight 数据库(https://db.dxy.cn/)
Insight数据库显示,目前国内尚无卡非佐米制剂获批上市,曾有国内仿制药企业报上市,但是最终获批临床,目前仿制药都处于批准临床阶段。
在一项代号为 ENDEAVOR 的 III 期研究中,按预定计划进行的总生存期(OS)中期分析结果显示,Kyprolis(卡非佐米)+地塞米松治疗复发或难治性多发性骨髓瘤患者相比 Velcade(硼替佐米)+地塞米松可使中位 OS 延长 7.6 个月(47.6 vs 40.0 个月)。

图片来源:Insight 数据库(https://db.dxy.cn/)
目前,国内企业在研卡非佐米的企业共有石药、豪森、正大天晴、重庆医工院、北京阳光诺和药物研究有限公司等 6 家,均处于批准临床的阶段。
2019 年 11 月,百济神州与安进达成合作,合作内容包括在中国开发和商业化安进的产品安加维®(XGEVA®)地舒单抗注射液、KYPROLIS®注射用卡非佐米和 BLINCYTO®注射用倍林妥莫双抗,以及在全球范围内共同开发 20 款安进抗肿瘤管线药物,其中百济神州将负责在中国的开发和商业化。
目前,双方合作的地舒单抗和倍林妥莫双抗均已在国内实现商业化,卡非佐米获批后将又实现一合作产品商业化落地。
