【通用名】Dabrafenib
【商品名】Tafinlar
【研发公司】葛兰素史克
【中文名】达拉非尼(甲磺酸达拉非尼胶囊)
【剂型规格】本品为胶囊剂,有50mg和75mg两种规格。
【活性成分】Dabrafenib甲磺酸盐
1 、适应证和用途
TAFINLAR®是适用于有不能切除或转移黑色素瘤。通过 FDA-批准的测试检验有 BRAF V600E 突变患者的治疗,使用限制:TAFINLAR 不适用有野生型 BRAF 黑色素瘤患者的治疗。
2 、剂量和给药方法
患者选择 开始用 TAFINLAR 治疗前确证肿瘤标本内存在 BRAF V600E 突变[见警告和注意事项(5.2)]。在 http://www.fda.gov/CompanionDiagnostics 可得到对 FDA 批准的为检测在黑色素瘤中 BRAF V600 突变测试信息。
推荐给药 TAFINLAR 的推荐剂量是 150 mg 口服每天 2 次,约 12 小时间隔,直至疾病进展或发生不能接 受的毒性。在进餐前至少 1 小时或后至少 2 小时服用丢失剂量可在下一次剂量前 6 小时服用。不要打开,压碎,或破坏 TAFINLAR 胶囊。
剂量修饰 对新原发性皮肤恶性病:无剂量修饰建议。

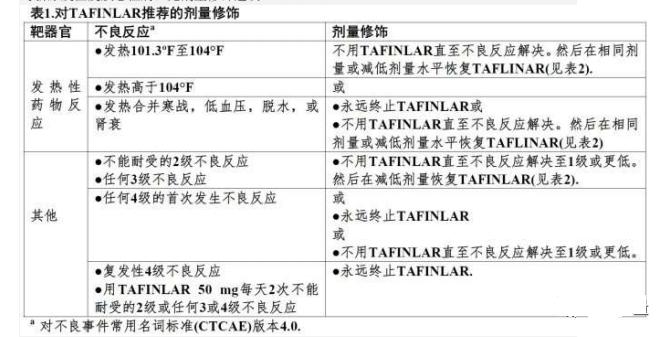
3 剂型和规格
50 mg 胶囊:深红色胶囊印有‘GS TEW’和‘50 mg’。75 mg 胶囊:深粉红色胶囊印有‘GS LHF’和‘75 mg’。
4 禁忌证
无。
5 可能存在不良影响:
最常见不良反应(≥20%):
角化过度,头痛,发热,关节炎,乳头状瘤,脱发,和掌跖红肿疼痛综合征。
新原发性皮肤恶性病
在 BRAF 野生型黑色素瘤中促肿瘤
严重发热性药物反应
高血糖
葡萄膜炎和虹膜炎
葡萄糖-6 磷酸脱氢酶缺乏
胚胎胎儿毒性
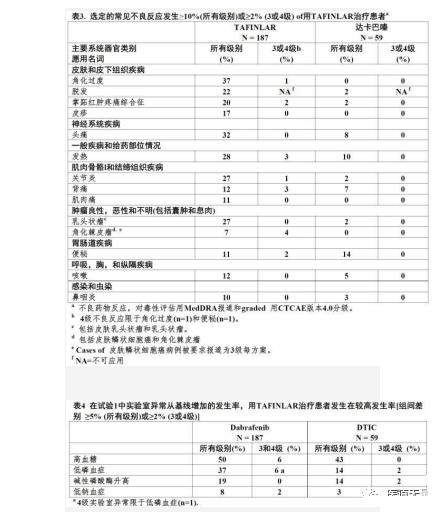
6 药物相互作用
其他药物对 Dabrafenib 的影响 抑 制或诱导药物-代谢酶的药物:Dabrafenib 主要地通过 CYP2C8 和 CYP3A4 被代谢。CYP3A4 或 CYP2C8 的强抑制剂或诱导剂分别可能 增加或减低 dabrafenib 的浓度[见临床药理学(12.3)]。用 TAFINLAR 治疗期间建议取代 CYP3A4 或 CYP2C8 的强抑制剂或强诱导 剂。
如强抑制剂的 同时使用(如,酮康唑[ketoconazole],奈法唑酮[nefazodone],克拉霉素[clarithromycin],吉 非贝 齐[gemfibrozil])或 CYP3A4 或 CYP2C8 的强诱导剂(如,利福平[rifampin],苯妥英[phenytoin], 卡马西平 [carbamazepine],苯巴比妥[phenobarbital],圣约翰草[St John’s wort])是不可避免,当 用强抑制剂密切监视患者不良反应或当用强诱导剂时丧失疗效。
影响胃 pH 药物:改变上胃肠道 pH 药物(如,质子泵抑制 剂,H2-受体拮抗剂,抗酸药)可能改 变 dabrafenib 的溶解度和减低其生物利用度。但是,未曾进行正式临床试验评价胃 pH-改变药对 dabrafenib 全身暴露的影响。当 TAFINLAR 与质子泵抑制剂,H2-受体拮抗剂,或抗酸药共同给 药,dabrafeni 的全身暴露可能减低和 不知道对 TAFINLAR 疗效的影响。
Dabrafenib 对其他药物的影响 Dabrafenib 诱导 CYP3A4 和可能诱导其他酶包括 CYP2B6,CYP2C8, CYP2C9,CYP2C19,和 UDP 葡萄糖醛酸转移酶(UGT)和可能诱导转运蛋白。Dabrafenib 减低咪达唑仑[midazolam](一种 CYP3A4 底物)的浓度(Cmax)和曲线下面积(AUC)分别为 61%和 74%[见临床药理学(12.3)]。
TAFINLAR 与这些酶的其他底 物同共给药,包括华法林[warfarin],地塞米松[dexamethasone], 或激素避孕药,可能导致减低浓度和丧失疗效[见在特殊人群中使用,如果不可避免 使用这些药物,取代这些药物或监视患者丧失疗效。
7、在特殊人群中使用
妊娠 妊娠类别 D 风 险总结:根据其作用机制,当给予妊娠妇女时 TAFINLAR 可能致胎儿危害。在大鼠中剂量根 据 AUC 大于推荐临床剂量 150 mg 每天 2 次时人暴露 3 倍时 Dabrafenib 是致畸胎和胚胎毒性。如此药妊娠期间使用或如当服用此药患者成为妊娠,应忠告患者对胎儿潜在危害
哺乳母亲 不知道此药是否存在于人乳汁中。因为许多药物存在于人乳汁和因为哺乳婴儿来自 TAFINLAR 严重不良反应潜能,应做出决策是否终止哺乳或终止药物,考虑药物对母亲的重要性。
儿童使用 尚未确定在儿童患者中 TAFINLAR 的安全性和有效性。
肝受损 在 有肝受损患者中未曾进行正式药代动力学试验。根据群体药代动力学分析的结果轻度肝受损 患者建议无需剂量调整。因为肝代谢和胆汁分泌是 dabrafenib 及其代谢物的消除主要途径,有中 度至严重肝受损患者可能增加暴露。对中度至严重肝受损患者尚未确定适宜剂量
肾受损 在有肾受损患者未曾进行正式药代动力学试验。根据群体药代动力学分析结果对有轻度或中度肾 受损患者建议无需调整剂量。对有严重肾受损患者尚未确定适宜剂量。
8、作用机制
abrafenib 是一种有些突变形式 BRAF 激酶的抑制剂。对 BRAF V600E,BRAF V600K,和 BRAF V600D 酶分别有体外 IC50 值 0.65,0.5,和 1.84 nM。Dabrafenib 还抑制野生型 BRAF 和 CRAF 激酶有 IC50 值分别为 3.2 和 5.0 nM,和其他激酶例如 SIK1,NEK11,和 LIMK1 在更高浓度。
在 BRAF 基因中有些突变,包括那些导致 BRAF V600E,可能导致组成性激活 BRAF 激酶可能 刺激肿瘤细胞生长在体外和体内 Dabrafenib 抑制 BRAF V600 突变阳性黑 色素瘤 细胞生长。
9、警告事项病变变化立即联系其医生:
TAFINLAR 致发热包括严重发热性药物反应。指导患者当服用 TAFINLAR 时如他们经受发热 联系其医生
在糖尿病患者 TAFINLAR 可能损害血糖控制导致需要更强化降血糖治疗。忠告患者联系其医 生报告严重高血糖症状。
有葡萄糖-6 磷酸脱氢酶(G6PD)缺乏患者 TAFINLAR 可能致溶血性贫血。忠告已知有 G6PD 缺 乏患者联系其医生报告贫血或溶血体征和症状。
如妊娠期间服用 TAFINLAR 可能致胎儿危害。指导女性患者治疗期间和治疗后 4 周使用非激 素,高效避孕。忠告患者当服用 TAFINLAR 如成为妊娠或如怀疑妊娠联系其医生 。
如哺乳期间母亲服用 TAFINLAR 哺乳婴儿可能经受严重不良反应。忠告哺乳母亲当服 TAFINLAR 时终止哺乳。
男性患者是处于对受损精子发生风险增加。
应在进餐前至少 1 小时或后至少 3 小时服 TAFINLA

