ジクロロニッケル(II) 化学特性,用途語,生産方法
外観
うすい赤黄色〜黄褐色, 粉末又は塊
性質
塩化ニッケルは、淡黄橙色の塊状、結晶、粉末であり、吸湿性があります。融点は1,001°Cです。一般的に広く用いられる六水和物の外観は、緑~黄緑の結晶です。潮解性があり、水やアルコールによく溶けます。
2価のニッケルは不対電子を2つ有し、平面4配位のニッケル錯体は反磁性を示します。
溶解性
水に易溶 (53.8g/100g, 0℃)。エタノールに易溶。水に極めて溶けやすく、エタノールに溶けやすい。
解説
NiCl2(129.60).ニッケルを塩素中で加熱すると得られる.ジクロロニッケル(II)は,黄色の潮解性りん片状晶.密度3.55 g cm-3.融点1001 ℃(封管中).973.4 ℃ で昇華する.水に易溶,エタノールに可溶.水溶液は鮮緑色で,蒸発濃縮すると六水和物が得られる.六水和物は緑色の潮解性りん片状晶.密度1.92 g cm-3.水,エタノールに易溶.ニッケルめっき浴,ガスマスク(アンモニアガス吸収剤),染料,電池,ニッケル金属,ニッケルせっけんの製造などに用いられる.森北出版「化学辞典(第2版)
用途
塩化ニッケル(II)(えんかニッケル(II)、nickel(II) chloride)は塩素とニッケルのイオン性化合物(塩)である。無水物の組成式は NiCl2 で、融点の高い常磁性を持つ黄色の固体である。ニッケル化合物としては最も広く使われており、ニッケルめっきなどに用いられる。
構造
塩化ニッケルの化学式は、NiCl2で表されます。無水塩の式量は129.59、比重は3.55であり、六水和物の式量は237.69、比重は1.92です。
結晶構造は、塩化カドミウムと同じです。それぞれのNi2+中心に6つのCl−イオンが配位し、それぞれのCl−は3つのNi2+と結合しています。Ni−Cl結合はイオン性です。
六水和物であるNiCl2•6H2Oは、水分子6つの中で4つだけがニッケルに直接結合しています。すなわち、錯体部分のtrans-[NiCl2(H2O)4]と錯体に弱く結合した水分子2つから構成される結晶構造を有します。
合成
塩化ニッケルの合成法
塩化ニッケルの製造方法には、金属ニッケル、、または炭酸ニッケルをに溶解して水和物を得た後、塩化水素の気流下で加熱して得る方法が知られています。
水和物は、加熱だけでは無水物になりません。緑から黄に色が変わるため、脱水が確認できます。
説明
Nickel chloride, NiCl2, is a water-soluble salt used in a variety
of industries. It is typically produced and used either as an
anhydrous salt or as a hydrate: nickel chloride hexahydrate as
well as nickel chloride dihydrate. Nickel chloride is very rarely
found in nature, and is produced via extraction from nickelcontaining
ores via treatment with hydrochloric acid.
化学的特性
Nickel chloride appears as green or brown
scales, or sparkling golden-yellow powder.
物理的性質
The anhydrous salt forms yellow crystal scales; deliquesces; density 3.55 g/cm
3; melts at 1,001°C; sublimes at 973°C; highly soluble in water, 64 g/100mL at 20°C; soluble in alcohol.
The hexahydrate forms green monoclinic crystals; deliquesces; extremely soluble in water, 254 g/100mL at 20°C, and about 600 g/100 ml at 100°C; also very soluble in alcohol.
使用
Nickel chloride solutions are used for electroplating nickel onto other metal items.It also is used to prepare various nickel salts and nickel catalysts; and in industrial gas masks to protect from ammonia.
定義
ChEBI: A compound of nickel and chloride in which the ratio of nickel (in the +2 oxidation state) to chloride is 1:2.
Nickel chloride is a yellow deliquescent solid with a boiling point of 973°C(1690°F). Nickel chloride is soluble in water and alcohol. Nickel chloride(hydrated),NiCI2·H20, is a gray deliquescent solid that is also soluble in water and alcohol.It is used in nickel plating.
調製方法
Nickel chloride (hexahydrate) is obtained by reacting metal
nickel powder or nickel oxide with hot, dilute hydrochloric
acid.
製造方法
Nickel(II) chloride can be obtained by reaction of the elements either in a flow
system at high temperatures or by reaction in ethanol at 20°. It is readily prepared in the laboratory by dehydration of the hexahydrate with thionyl chloride.
一般的な説明
Nickel(II) chloride (NiCl
2) is a nickel based halide that is prepared by burning nickel in chlorine. It is a water soluble compound that crystallizes to form a hexahydrate. It is majorly utilized in organic synthesis as a catalyst and a precursor.
危険性
Confirmed carcinogen.
使用用途
工業的に塩化ニッケルは、アンモニアガス吸収剤、、染料、電池などに用いることが可能です。錯体化学ではニッケル錯体のとして、さらに有機合成で添加剤や試薬としても広く知られています。
特に大部分は、ニッケルめっきに使用されており、陽極の金属ニッケルを溶かし、さらに液の溶解度を増やす働きがあります。すなわち、めっき浴ではニッケルイオンの供給源です。
その一方で、塩化物イオンを共有する役割を持っており、塩化物イオンの腐食性で陽極のニッケルがイオンとして溶解を促進します。
関連する反応
塩化ニッケルを用いた反応
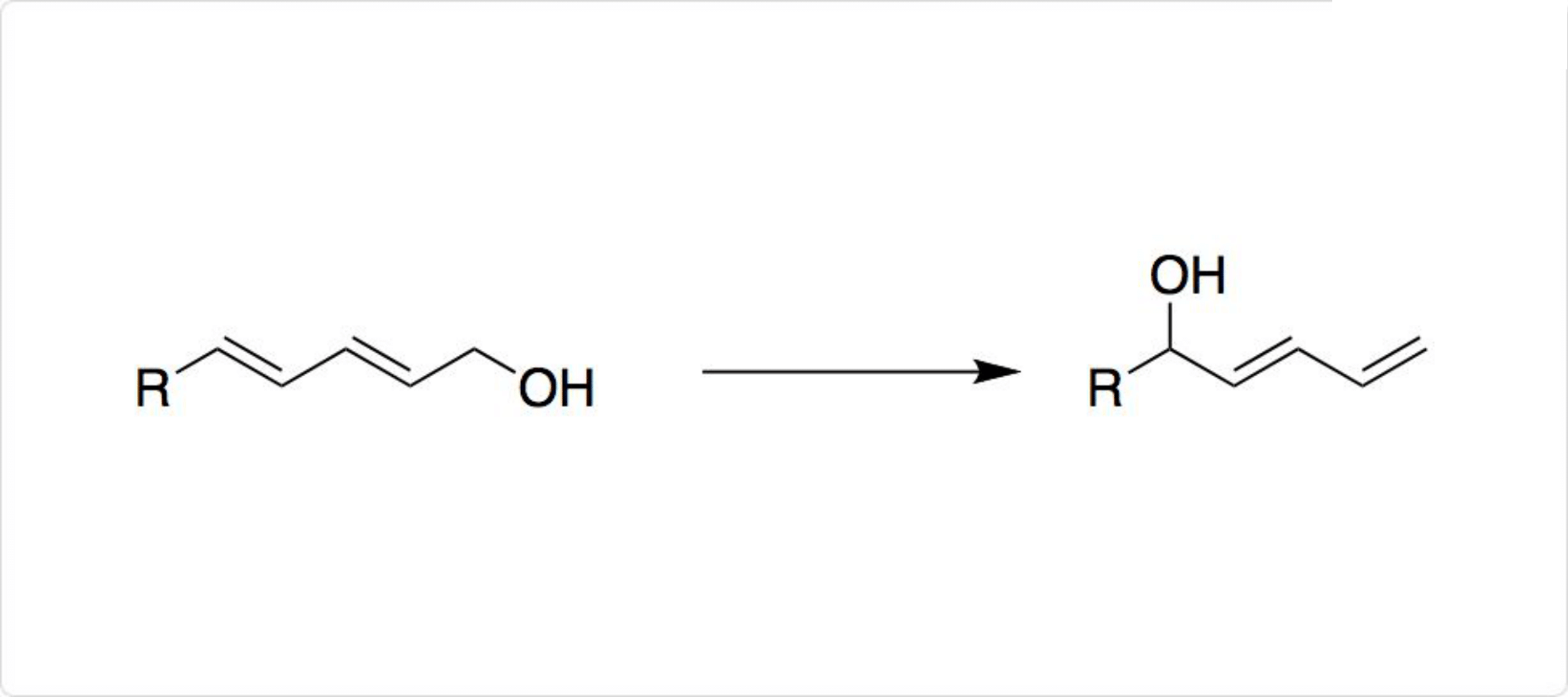
図1. 塩化ニッケルを用いた反応
塩化ニッケルや水和物は、さまざまな有機合成反応に利用可能です。例えば、弱いルイス酸として、ジエノールの位置異性化に用いられます。
塩化クロム(II) (CrCl2) と組み合わせて、ヨウ化ビニル化合物とアルデヒドからアリルアルコールを合成できます。水素化リチウムアルミニウム (LiAlH4) での還元での添加剤のほか、水素化ホウ素ナトリウム (NaBH4) の反応でのホウ化ニッケルの調製などにも使用可能です。
安全性プロファイル
Confirmed human
carcinogen. Poison by ingestion,
intravenous, intramuscular, and
intraperitoneal routes. An experimental
teratogen. Experimental reproductive
effects. Mutation data reported. When
heated to decomposition it emits very toxic
fumes of Cl-. See also NICICEL
COMPOUNDS.
職業ばく露
Nickel chloride is used in electroplating
and ink manufacturing.
環境運命予測
Nickel chloride is water soluble (642 g l
-1 for anhydrous;
2540 g l
-1 for hexahydrate) and would be expected to release
divalent nickel into the water. Since nickel chloride quickly
dissolves upon exposure to moist environments, and partially
due to the ubiquity of nickel in soil, water, and air, tracking the
course of the salt through the environment is difficult. This is
particularly due to nickel’s ability to complex with anionic
species other than chloride to form nickel oxide, sulfate, nitrate,
carbonate, or acetate, among others.
Industrial uses of nickel chloride result in nickel being
distributed mainly at soil surfaces and through surrounding
waterways and water tables. Once distributed to the soil, nickel
chloride produces nickel(II) ions to potentially form inorganic
crystalline minerals or precipitates, can complex or adsorb onto
organic and inorganic surfaces, can participate in cation
exchange, and can exist as free-ion or chelated metal complexes
in soil solution.
輸送方法
UN3288 Toxic solids, inorganic, n.o.s., Hazard
Class: 6.1; Labels: 6.1-Poisonous materials, Technical
Name Required.
純化方法
It crystallises from dilute HCl to form the green hexahydrate. At 70o this dehydrates to the tetrahydrate, and at higher temperatures it forms the anhydrous salt. It sublimes in yellow hexagonal scales in a stream of HCl. Store it in a desiccator as it is deliquescent. [Hart & Partington J Chem Soc 104 1943.]
不和合性
Strong acids, potassium, sulfur. Forms
an impact-sensitive mixture with potassium.
廃棄物の処理
Recycle or disposal in a
chemical waste landfill is recommended.
参考文献
A. Ferrari, A. Braibanti, G. Bigliardi, Acta Crystallogr., 16, 846 (1963), DOI: 10.1107/S0365110X6300222X.
ジクロロニッケル(II) 上流と下流の製品情報
原材料
準備製品