Natrium-4-(2,4-dihydroxyphenyl-azo)benzolsulfonat Chemische Eigenschaften,Einsatz,Produktion Methoden
Beschreibung
Methylorange ist ein intensiv orangegelbes Pulver, das in Wasser nur begrenzt (löst sich in 500 Teilen Wasser) und in Ethanol sehr schwer löslich ist. Dieser Azofarbstoff weist eine gute Lichtechtheit auf, ist aber sehr säureempfindlich, was die Verwendung als Indikator begründet. Methylorange ist ein Verwandter des Methylrots, welchem die SO3Na-Gruppe fehlt und stattdessen eine COOH-Gruppe in 2-Position des Benzolkerns aufweist. Typisch ist der Einsatz von Methylorange als Indikator mit dem Umschlagsbereich pH 3.0 - 4.4. Hierbei kommt es zu einem Farbwechsel von Rot nach Gelborange. Verwendet werden sehr verdünnte Lösungen in Wasser oder 20%-igem Ethanol (z.B. 0.04 g Methylorange in jeweils 100 ml dieser Lösungsmittel), der Indikator dient insbesondere zur acidimetrischen Titration von Mineralsäuren.
Synthese
Schritt 1: sulfanilsaures Natrium (Natriumsalz der Sulfanilsäure) [515-74-2] C6H6NO3Na
In einem 250-ml-Rundkolben versetzt man 50 g konzentrierte Schwefelsäure langsam unter Umrühren mit 50 g frisch destilliertem Anilin und erhitzt im Ölbad etwa 6 Stunden auf 180-200 °C, bis eine mit Wasser verdünnte Probe auf Zusatz von Natronlauge kein Anilin mehr abscheidet. Das Reaktionsprodukt wird mit 20 g Natriumhydroxid in nicht verdünnter Lösung versetzt, worauf Lösung erfolgt. Das Filtrat neutralisiert man mit Salzsäure, kocht nach Zugabe von etwas Kohle 15 Minuten lang und filtriert. Nach dem Erkalten scheiden sich Kristalle in Form von leicht löslichen Tafeln aus.
Schritt 2: Methylorange
22 g sulfanilsaures Natrium werden in 100 ml Wasser suspendiert, mit Eisessig angesäuert und mit 12 g Dimethylanilin zur Lösung gebracht. Nunmehr lässt man unter Eiskühlung eine Lösung von 8 g Natriumnitrit in 100 ml Wasser zufließen. Methylorange scheidet sich dann in orangefarbenen, kristallinen Blättchen aus. Zur vollständigen Fällung wird Natronlauge bis zur deutlich alkalischen Reaktion hinzugegeben. Den Niederschlag saugt man nach einigen Stunden ab und kristallisiert aus Wasser um. Die Ausbeute ist nahezu theoretisch.
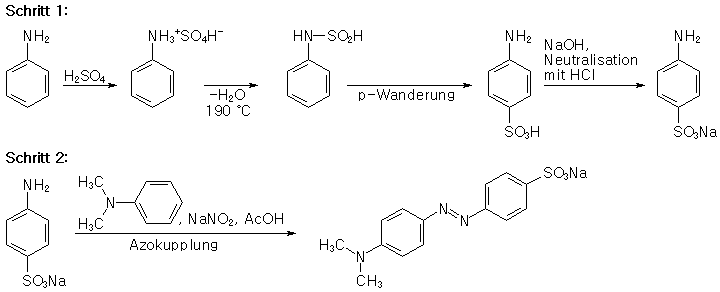
Zur Reaktion
Im ersten Schritt wird Anilin mit konzentrierter Schwefelsäure in Sulfanilsäure überführt. Dabei entsteht, wenn man äquimolekulare Mengen Anilin und konz. Schwefelsäure verwendet, zunächst das saure Sulfat des Anilins, welches beim Erhitzen auf 180° C unter Wasserabspaltung in die Phenylaminsulfamidsäure übergeht. Die Sulfonsäuregruppe wandert dann aus der Seitenkette in die p-Stellung (und o-Stellung) des Kerns. Im zweiten Schritt wird Methylorange durch Kuppeln von diazotierter Sulfanilsäure mit N,N-Dimethylanilin hergestellt.
Quelle
Winterfeld, K. - Praktikum der organisch-präparativen Pharmazeutischen Chemie, 4. Auflage
R-Sätze Betriebsanweisung:
R25:Giftig beim Verschlucken.
R10:Entzündlich.
S-Sätze Betriebsanweisung:
S45:Bei Unfall oder Unwohlsein sofort Arzt zuziehen (wenn möglich, dieses Etikett vorzeigen).
S24/25:Berührung mit den Augen und der Haut vermeiden.
S16:Von Zündquellen fernhalten - Nicht rauchen.
S36/37/39:Bei der Arbeit geeignete Schutzkleidung,Schutzhandschuhe und Schutzbrille/Gesichtsschutz tragen.
Aussehen Eigenschaften
C14H14N3NaO3S; Helianthin, Orange III, 4-(4-Dimethylamino)-phenylazo-benzolsulfonsäure Natriumsalz. Oranger Feststoff mit schwachem Eigengeruch.
Gefahren für Mensch und Umwelt
Giftig beim Verschlucken. Steht im Verdacht, Krebs zu erzeugen.
Brennbar.
Schutzmaßnahmen und Verhaltensregeln
Schutzhandschuhe als kurzzeitiger Staubschutz.
Verhalten im Gefahrfall
Vorsichtig trocken aufnehmen. Der Entsorgung zuführen. Nachreinigen.
Wasser.
Brennbar. Im Brandfall können Schwefeloxide und Stickoxide entstehen.
Erste Hilfe
Nach Hautkontakt: Mit reichlich Wasser abwaschen.
Nach Augenkontakt: Mit reichlich Wasser bei geöffnetem Lidspalt mindestens 15 Minuten ausspülen. Sofort Augenarzt hinzuziehen.
Nach Einatmen: Frischluft.
Nach Verschlucken: Reichlich Wasser trinken lassen. Erbrechen auslösen. Arzt hinzuziehen.
Nach Kleidungskontakt: Kontaminierte Kleidung entfernen.
Ersthelfer: siehe gesonderten Anschlag
Sachgerechte Entsorgung
Gelöst in z.B. Ethanol als halogenfreie, organische Lösemittelabfälle.
Chemische Eigenschaften
Orange-yellow powder. Soluble in hotwater; insoluble in alcohol.
Verwenden
Methyl orange is a pH indicator frequently used in titrations, also used for histological microscopy.
synthetische
4-Aminobenzenesulfonic acid diazo, and N,N-dimethylaniline coupling.
Definition
An acid–base indicator
that is red in solutions below a pH of 3 and
yellow above a pH of 4.4. As the transition
range is clearly on the acid side, methyl orange
is suitable for the titration of an acid
with a moderately weak base, such as
sodium carbonate.
Allgemeine Beschreibung
Orange powder.
Air & Water Reaktionen
Azo dyes can be explosive when suspended in air at specific concentrations. Insoluble in water.
Reaktivität anzeigen
Methyl Orange is an azo compound. Azo, diazo, azido compounds can detonate. This applies in particular to organic azides that have been sensitized by the addition of metal salts or strong acids. Toxic gases are formed by mixing materials of this class with acids, aldehydes, amides, carbamates, cyanides, inorganic fluorides, halogenated organics, isocyanates, ketones, metals, nitrides, peroxides, phenols, epoxides, acyl halides, and strong oxidizing or reducing agents. Flammable gases are formed by mixing materials in this group with alkali metals. Explosive combination can occur with strong oxidizing agents, metal salts, peroxides, and sulfides.
läuterung methode
Recrystallise it twice from hot water, then wash it with a little EtOH followed by diethyl ether. It is an indicator: pH 3.1 (red) and pH 4.4 (yellow). [Beilstein 16 IV 510.]
Natrium-4-(2,4-dihydroxyphenyl-azo)benzolsulfonat Upstream-Materialien And Downstream Produkte
Upstream-Materialien
Downstream Produkte

